Cho 18 gam hỗn hợp gồm Fe, Cu vào 200 ml dung dịch chứa NaNO3 1M và HCl 2M. Kết thúc phản ứng, nhỏ tiếp V ml dung dịch HCl 1M vào đó thì kim loại vừa tan hết. Biết trong dung dịch thu được không còn ion NO3- và NO là sản phẩm khử duy nhất. Giá trị của V và phần trăm khối lượng của Fe trong hỗn hợp ban đầu lần lượt là ?
400 và 46,67%.
400 và 31,11%.
200 và 46,67%.
200 và 31,11%.
Phân tích hiện tượng:
Khi cho hỗn hợp kim loại Fe và Cu vào dung dịch chứa H+ và NO3- thu được Fe2+, Cu+, NO( vì ngoài ra kim loại còn dư nên dung dịch thu được chứa Fe2+). Sau đó cho thêm H+ để kim loại tan hết (kim laoij có thể là Fe, Cu) thì kim loại dư phản ứng trước rồi đến Fe2+ (xét về tính khử) và sản phẩm tạo ra chỉ là Fe2+ và Cu2+ thì thỏa mãn đề bài: tan vừa hết.
![]()
Để kim loại tan vừa hết như trên thì ![]()
![]() nHCl thêm vào 0,8 – 0,4 = 0,4
nHCl thêm vào 0,8 – 0,4 = 0,4
![]() V = 400 (ml)
V = 400 (ml)
Gọi số mol Fe và Cu lần lượt là x và y.
Do đó 56x + 64y = 18 (1)
Theo định luật bảo toàn mol electron có: 2nFe + 2nCu = 3nNO hay 2x + 2y =0,6 (2)
Từ (1) và (2) suy ra x = y =0,15
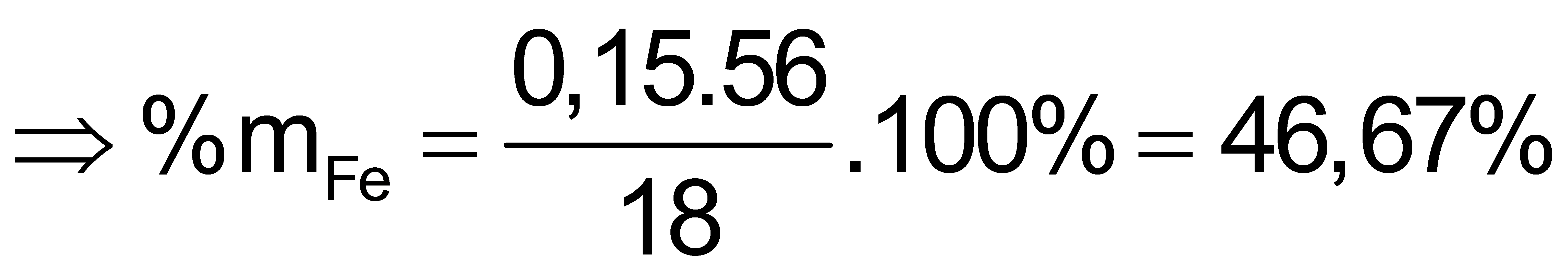
Vậy đáp án đúng là A
Chú ý: Cần nhớ các công thức về H+ và ![]() áp dụng cho trường hợp kim loại hoặc hỗn hợp kim loại phản ứng với HNO3:
áp dụng cho trường hợp kim loại hoặc hỗn hợp kim loại phản ứng với HNO3: ![]()
