Cho 6,72 gam Fe vào 400ml dung dịch HNO3 1M, đến khi phản ứng xảy ra hoàn toàn, thu được khí NO (sản phẩm khử duy nhất) và dung dịch X. Dung dịch X có thể hòa tan tối đa m gam Cu. Giá trị của m là:
1,92.
0,64.
3,84.
3,20.
1,92.
nFe = ![]() =0,12 (mol);
=0,12 (mol); ![]() = 0,4 (mol).
= 0,4 (mol).
Cách 1: Nếu tạo muối sắt (III) thì ta có phương trình:
![]() (1)
(1)
Vậy sau phản ứng (1), Fe còn dư (nFe còn = 0,12 - 0,1 = 0,02 mol) sẽ phản ứng với Fe(NO3)3:
Fe + 2Fe(NO3)3 ![]() 3Fe(NO3)2 (2)
3Fe(NO3)2 (2)
0,02 ← 0,04 0,06
![]() Sau khi phản ứng (2) dung dịch X thu được có
Sau khi phản ứng (2) dung dịch X thu được có ![]()
Khi thêm Cu vào thì:
Cu + 2Fe(NO3)3 ![]() Cu(NO3)2 + 2Fe(NO3)2
Cu(NO3)2 + 2Fe(NO3)2
0,03 ← 0,06
nCu = 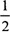 .
.![]() còn lại =
còn lại = 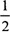 .0,06 = 0,03 mol
.0,06 = 0,03 mol ![]() mCu = 64.0,03 = 1,92 (gam).
mCu = 64.0,03 = 1,92 (gam).
Cách 2: Cu khi tan trong dung dịch X sẽ tạo muối sắt (II). Vậy ta có các quá trình oxi hóa và khử là:
Fe ![]() Fe2+ + 2e
Fe2+ + 2e ![]() + 3e + 4H+
+ 3e + 4H+ ![]() NO + 2H2O
NO + 2H2O
Cu ![]() Cu2+ + 2e
Cu2+ + 2e
Từ nH+= ![]() = 0,4 mol
= 0,4 mol ![]() ne (nhận) = 0,3 mol.
ne (nhận) = 0,3 mol.
Áp dụng bảo toàn electron ta có:
2nFe + 2nCu = 0,3 ![]() nCu =
nCu = ![]() = 0,03 mol
= 0,03 mol
![]() mCu= 64.0,03 = 1,92 (gam).
mCu= 64.0,03 = 1,92 (gam).
