Cho 8,64 gam Mg vào dung dịch hỗn hợp NaNO3 và H2SO4, đun nhẹ đến khi phản ứng xảy ra hoàn toàn thu được dung dịch A; 1,792 lít (đktc) hỗn hợp khí B có khối lượng 1,84 gam gồm 2 khí không màu có một khí hóa nâu và còn lại 4,08 gam chất rắn không tan. Cô cạn cẩn thận dung dịch A thu được m gam muối khan. Giá trị m là
A. 31,5 gam
B. 29,72 gam
C. 36,5 gam
D. 29,0 gam
nMg = 3 chất rắn không tan là Mg dư nMg (dư) 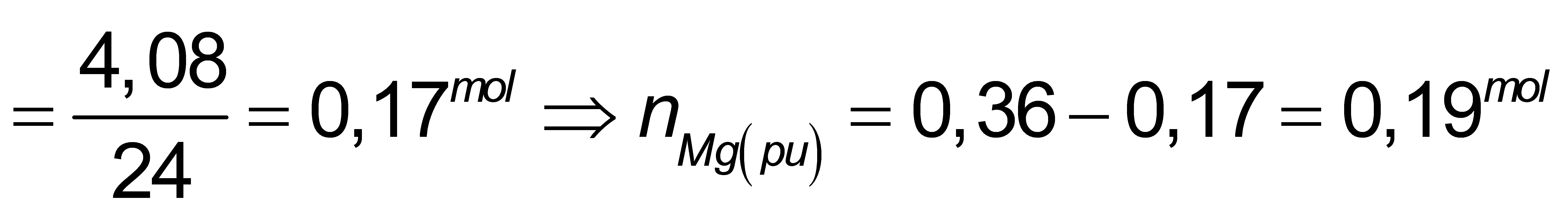
→ nelectron nhường = ![]()
Mtrung bình khí = 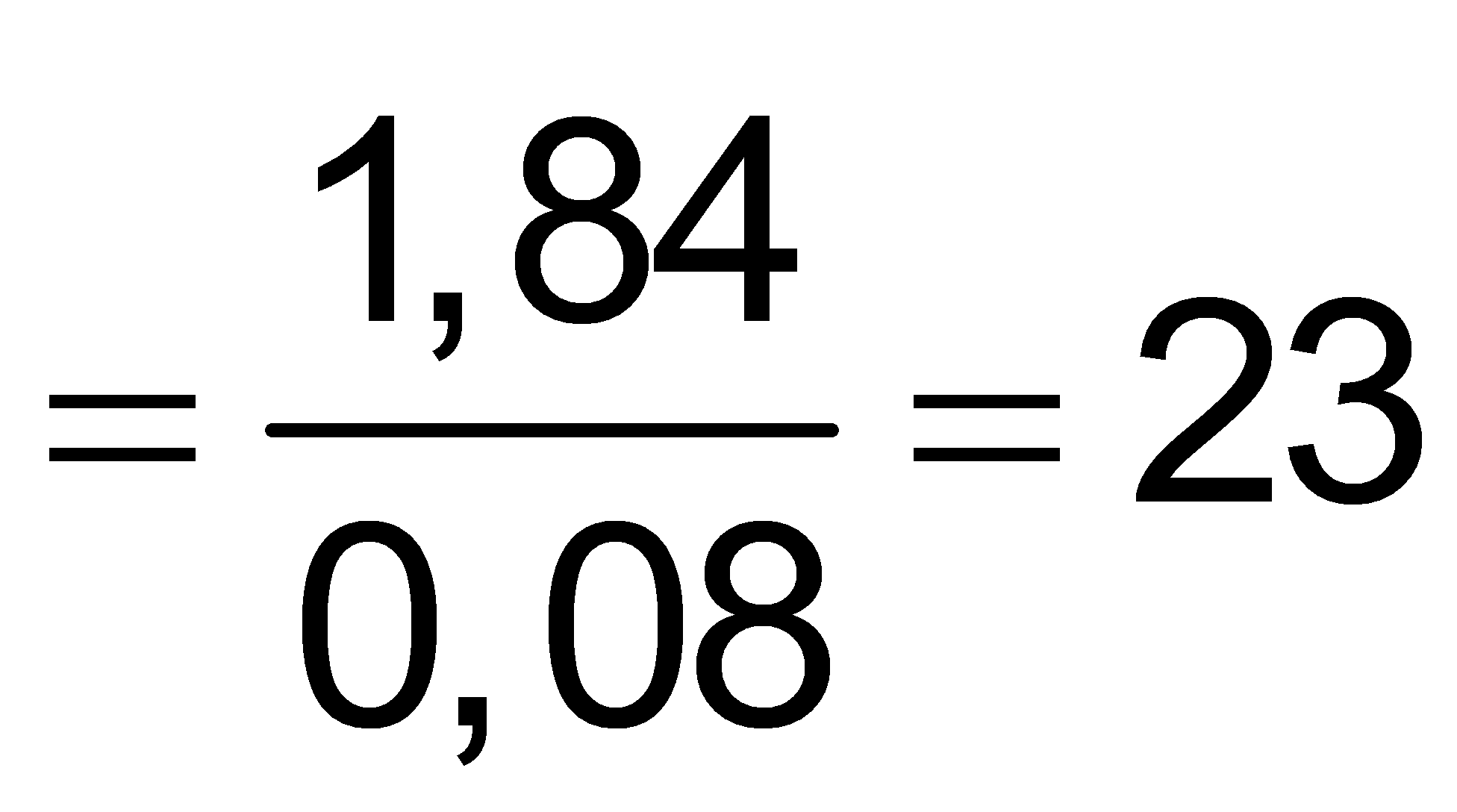 mà
mà ![]() nên khí còn lại có M < 23 chỉ có thể là H2
nên khí còn lại có M < 23 chỉ có thể là H2
Theo đường chéo ta có:
→ nelectron nhận tạo khí ![]()
![]() 0,19 0,38
0,19 0,38 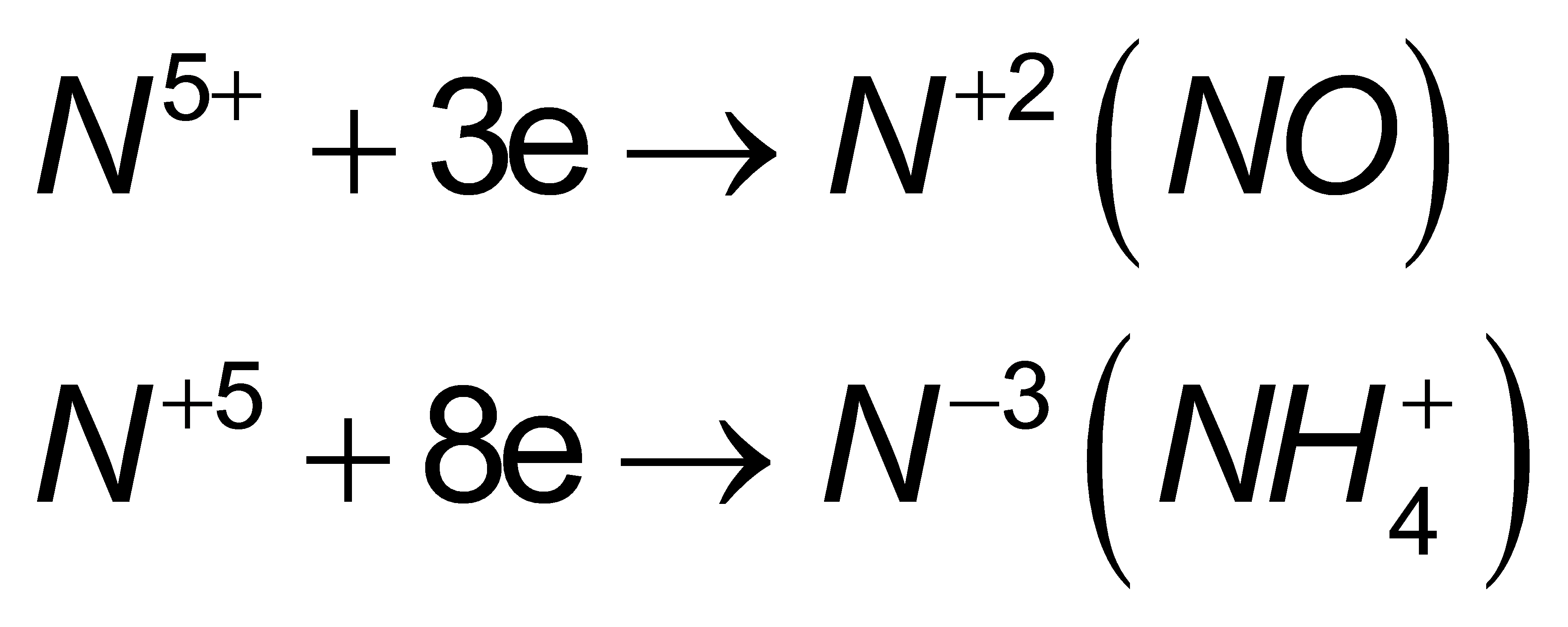 8x x
8x x ![]()
Bào toàn electron 0,38=0,06.3+8x+0,02.2 ⇒x=0,02
⇒ mmuối ![]()
Vậy đáp án đúng là B

 đều không xảy ra hoán vị gen.
đều không xảy ra hoán vị gen.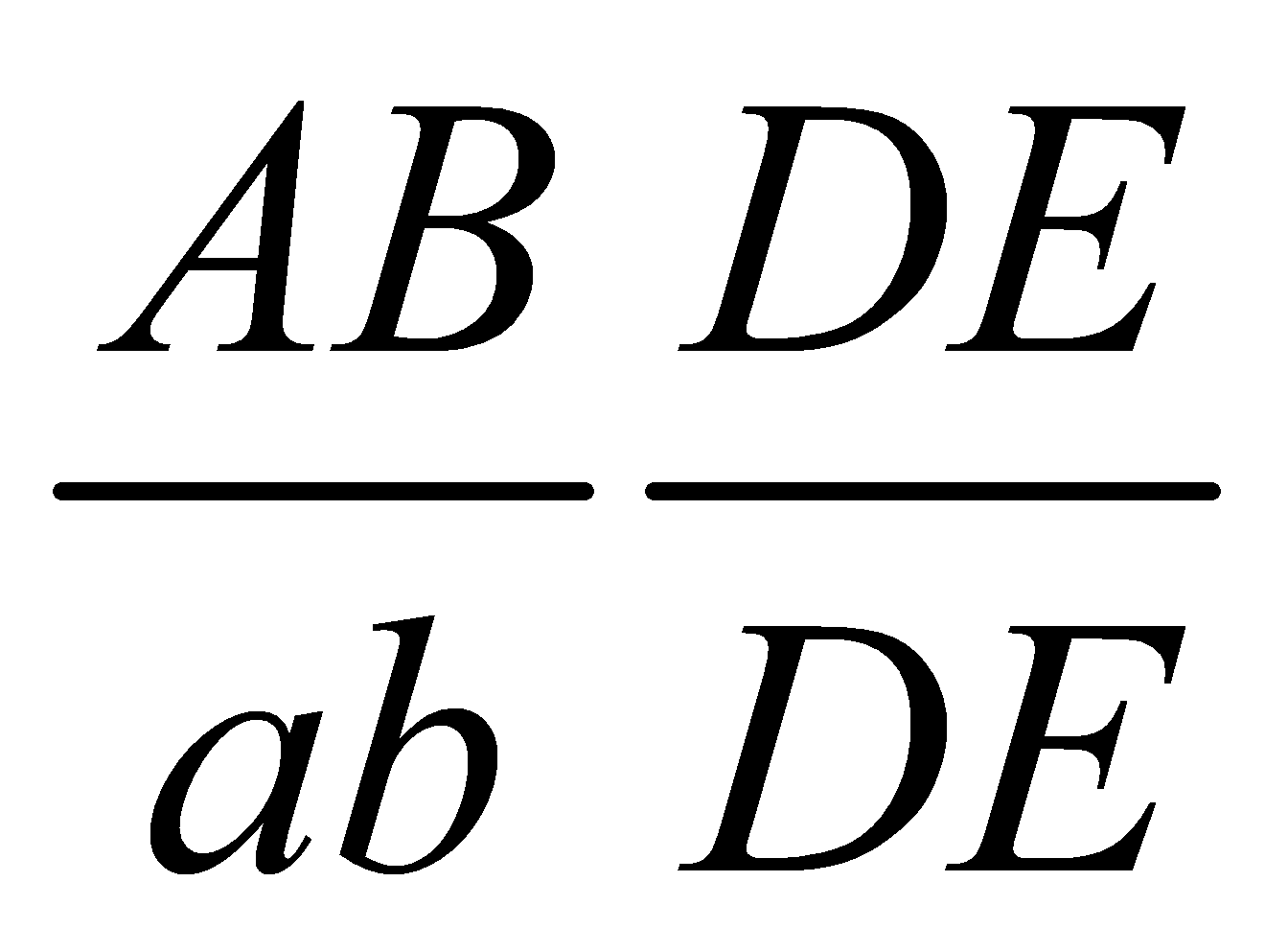 biết khoảng cách giữa gen A và gen B là 40cM. Các tế bào sinh tinh của cá thể trên giảm phân bình thường hình thành giao tử, theo lý thuyết trong số các loại giao tử được tạo ra, loại giao tử abDE chiếm tỉ lệ:
biết khoảng cách giữa gen A và gen B là 40cM. Các tế bào sinh tinh của cá thể trên giảm phân bình thường hình thành giao tử, theo lý thuyết trong số các loại giao tử được tạo ra, loại giao tử abDE chiếm tỉ lệ: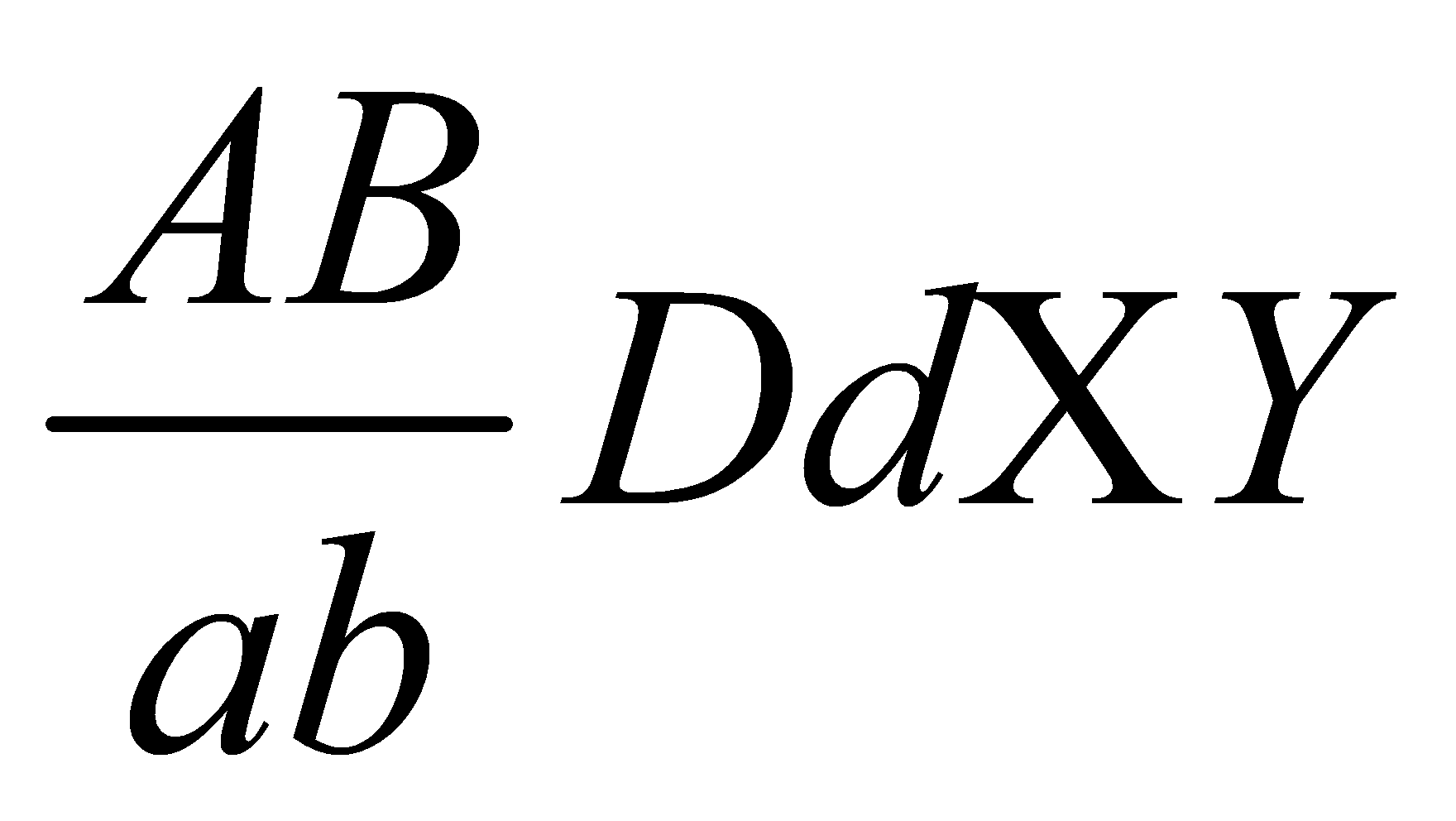 giảm phân bình thường hình thành các giao tử. Số loại giao tử tối đa có thể thu được là:
giảm phân bình thường hình thành các giao tử. Số loại giao tử tối đa có thể thu được là: