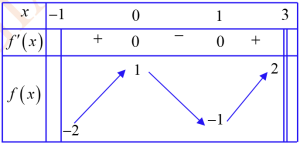
Cho x mol hỗn hợp kim loại Al, Fe (có tỉ lệ mol 1:1) tan hết trong dung dịch chứa Y mol HNO3 ( Tỷ lệ x:y = 3:17). Sau khi kim loại tan hết, thu được sản phẩm khử Y duy nhất và dung dịch Z chỉ chứa muối nitrat. Cho AgNO3 đến dư vào Z, thu được m gram rắn. Giá trị của m là :
A: 53y/17
B: 27y/17
C: 108y/17
D: 432y/17
Cho x=3; y=17 → nFe=nAl = ![]() =1,5 (mol)
=1,5 (mol)
Khi cho AgNO3 vào dung dịch Z thì tạo thành chất rắn do có phản ứng
![]()
Gọi nAg = a.
Bảo toàn e từ đầu đến cuối cùng ta có: 3nFe + 3nAl = nAg + nelectron mà N trao đổi → nelectron mà N trao đổi = 9 – a(mol)
Dung dịch cuối cùng có Fe(NO3)3; Al(NO3)3 trong đó có a mol ![]() do muối AgNO3 cung cấp.
do muối AgNO3 cung cấp.
Bảo toàn nguyên tố N ta có:
![]() =nN trong khí + nN trong muối = x(9-a) + (9-a)
=nN trong khí + nN trong muối = x(9-a) + (9-a)
Trong đó x là tỉ lệ giữa số nguyên tử N trong phân tử khí và số e mà một phân tử khí trao đổi.
Có 0 < a < 1,5 → 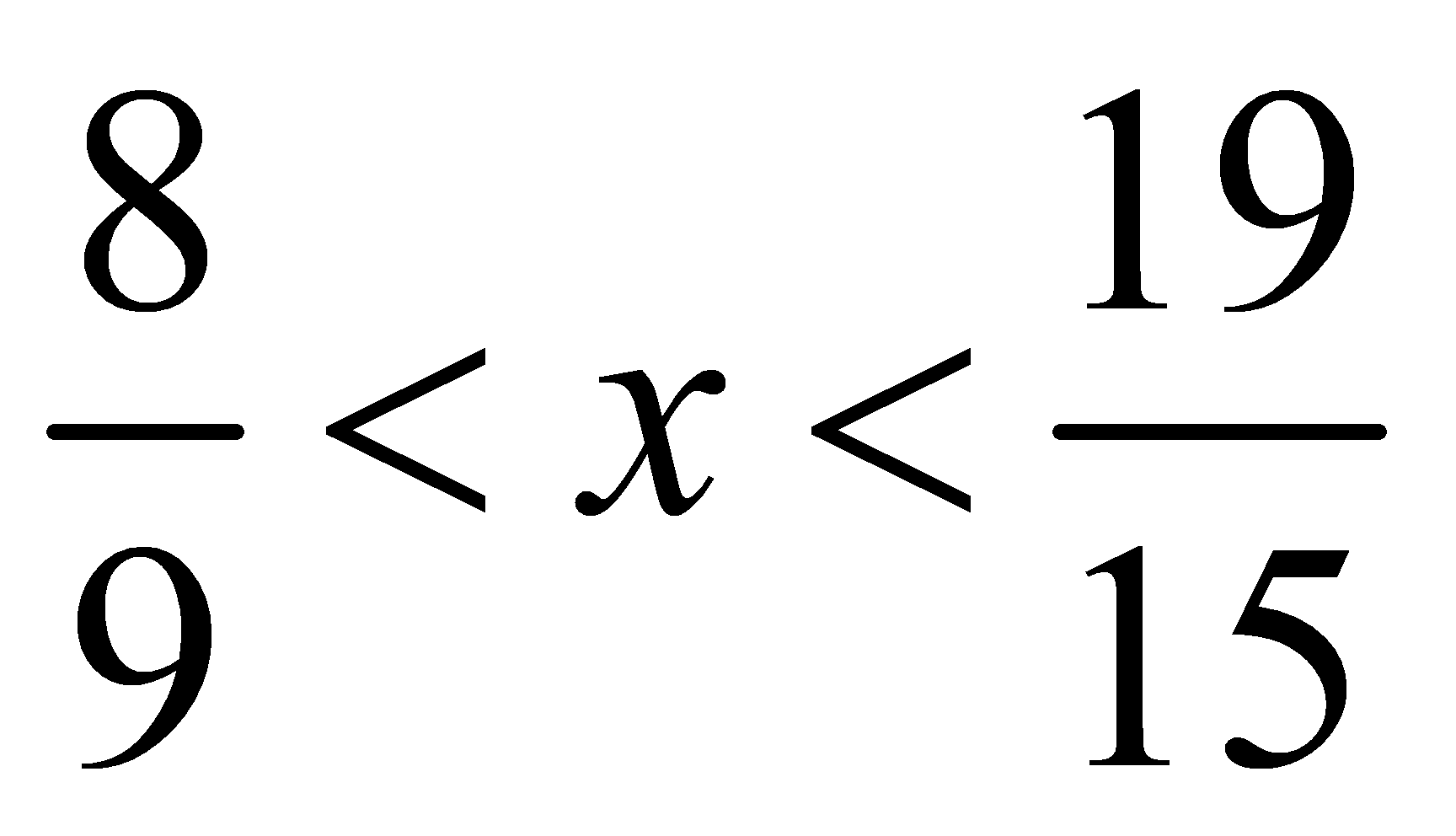
Dễ thấy chỉ có x=1 thỏa mãn →a=0,5 →m = 54 =![]()
Vậy đáp án đúng là A