Để hòa tan hoàn toàn 19,225 gam hỗn hợp X gồm Mg, Zn cần dùng vừa đủ 800 ml HNO3 1,5M. Sau khi phản ứng kết thúc thu được dung dịch Y và 2,24 lít (đktc) hỗn hợp khí A gồm N2, N2O, NO, NO2 (trong đó N2O và NO2 có số mol bằng nhau) có tỉ khối với H2 là 14,5. Phần trăm về khối lượng của Mg trong X là
A: 37,45%
B: 90,54%
C: 87,45%
D: 62,55%
Nhận thấy N2O = NO2= 2NO → quy hỗn hợp khí về NO : x và N2 : y Ta có hệ  Có 4n + 12nN2 = 0.05. 16 < nHNO3 = 1,2 mol → chứng tỏ sinh ra NH4NO3 nNH4NO3 =
Có 4n + 12nN2 = 0.05. 16 < nHNO3 = 1,2 mol → chứng tỏ sinh ra NH4NO3 nNH4NO3 = 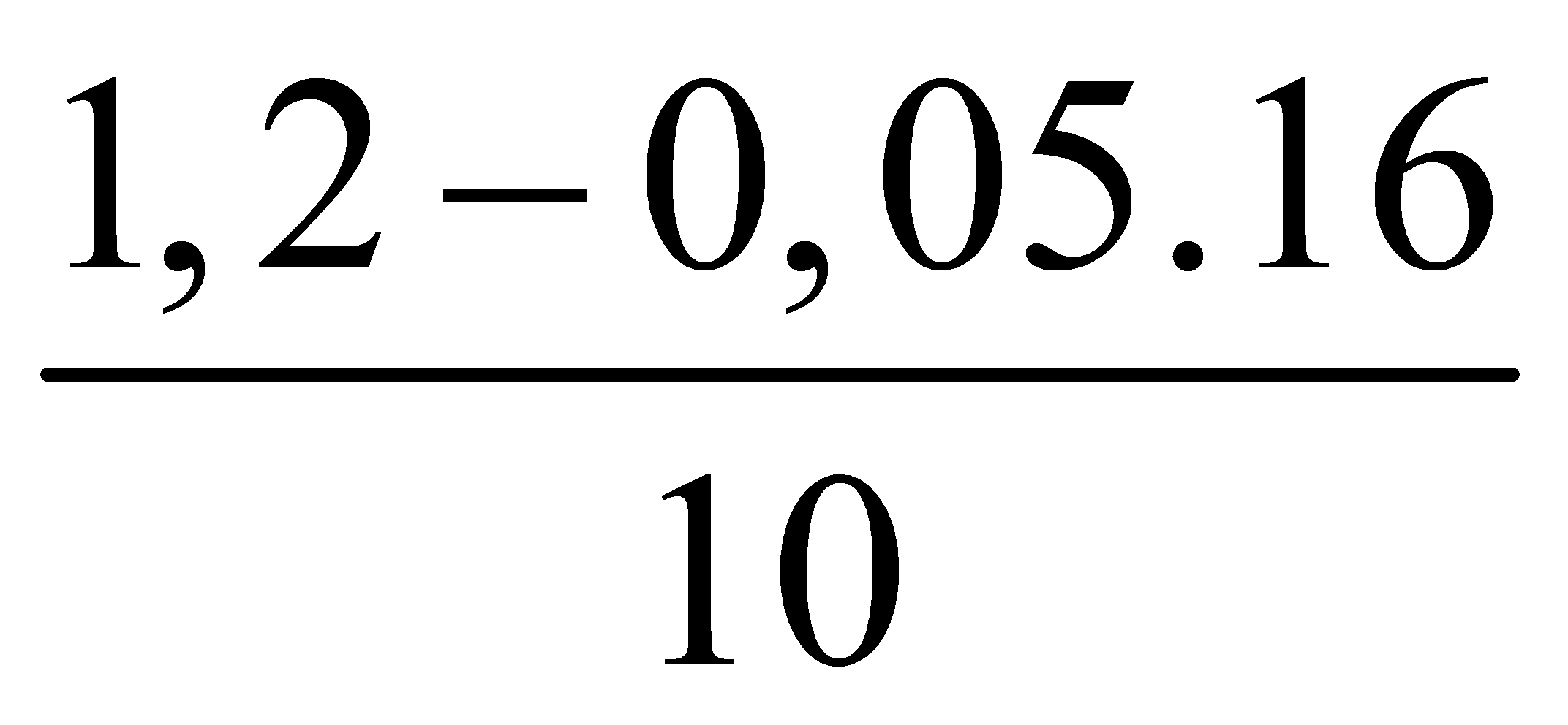 = 0,04 mol Gọi số mol của Mg và Zn lần lượt là a, b Ta có hệ
= 0,04 mol Gọi số mol của Mg và Zn lần lượt là a, b Ta có hệ 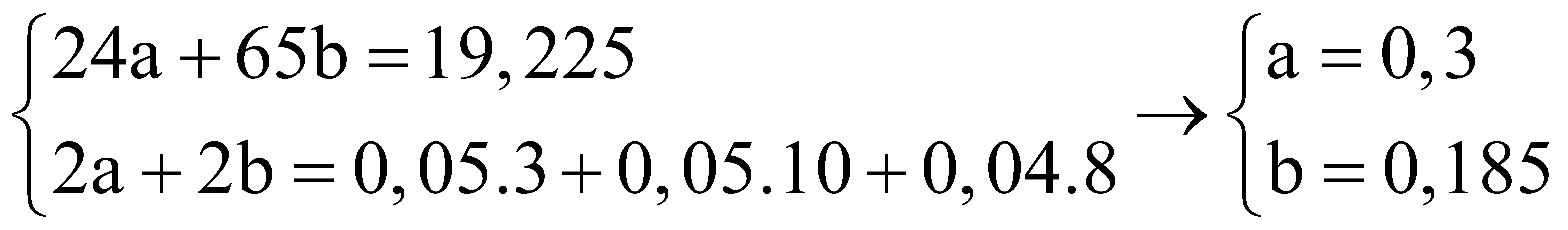 % Mg =
% Mg =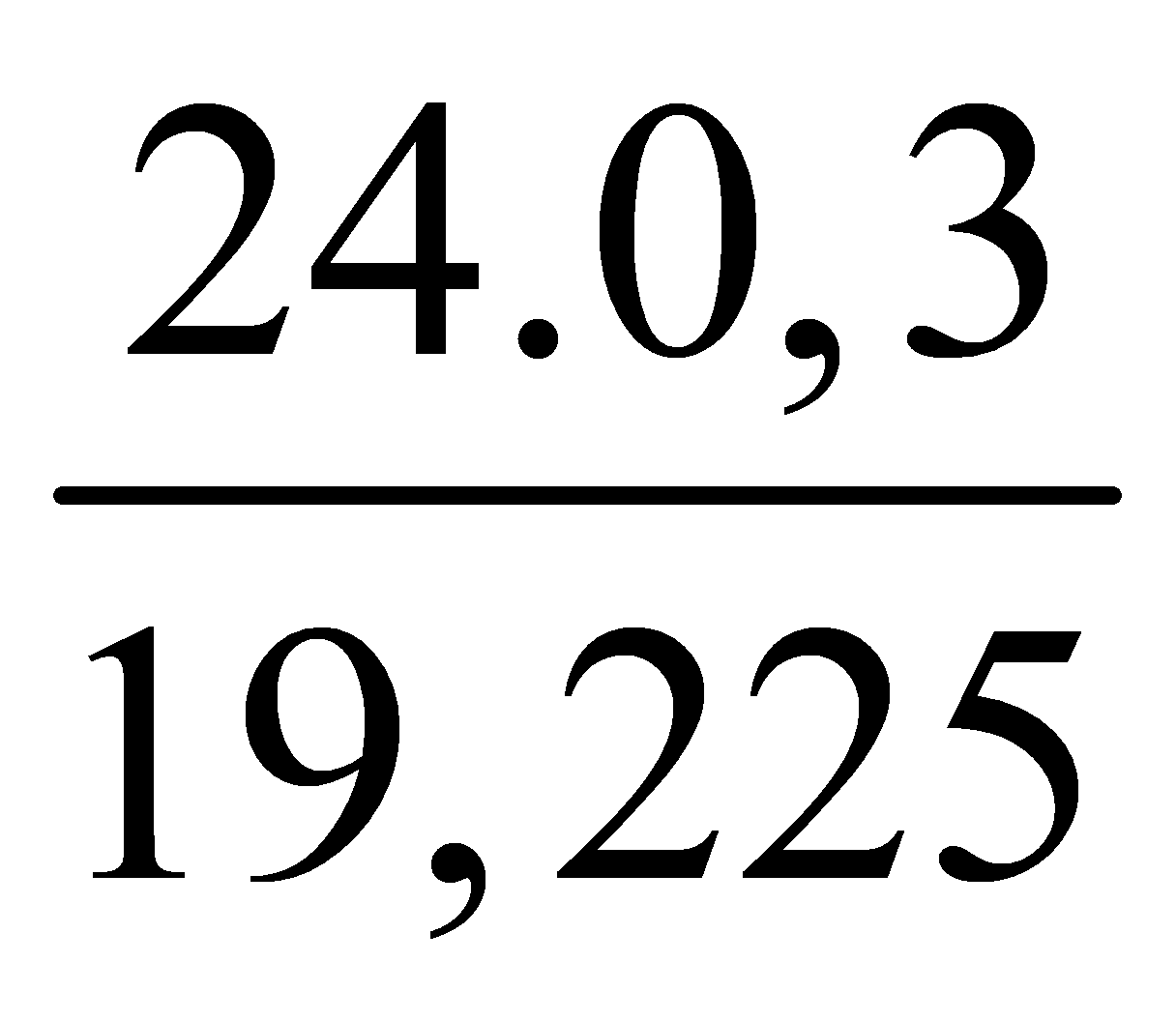 .100% = 37,45%.
.100% = 37,45%.
Vậy đáp án đúng là A
