Điện phân dung dịch chứa 0,2 mol CuSO4 và 0,12 mol NaCl bằng điện cực trơ, với cường độ dòng điện không đổi I=5A trong thời gian 4632 giây thì dừng điện phân. Nhúng thanh Mg vào dung dịch sau điện phân, kết thúc phản ứng, khối lượng thanh Mg thay đổi như thế nào so với trước phản ứng?
Giảm 3,36 gam.
Tăng 3,20 gam.
Tăng 1,76 gam.
Không thay đổi.
Số mol các chất và ion trong dung dịch ban đầu là: 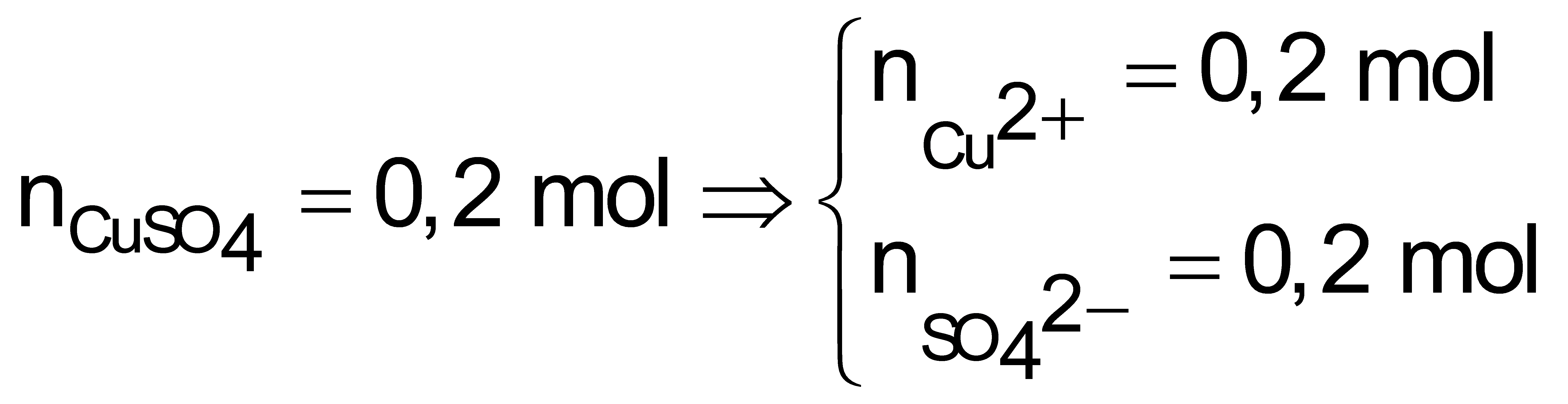
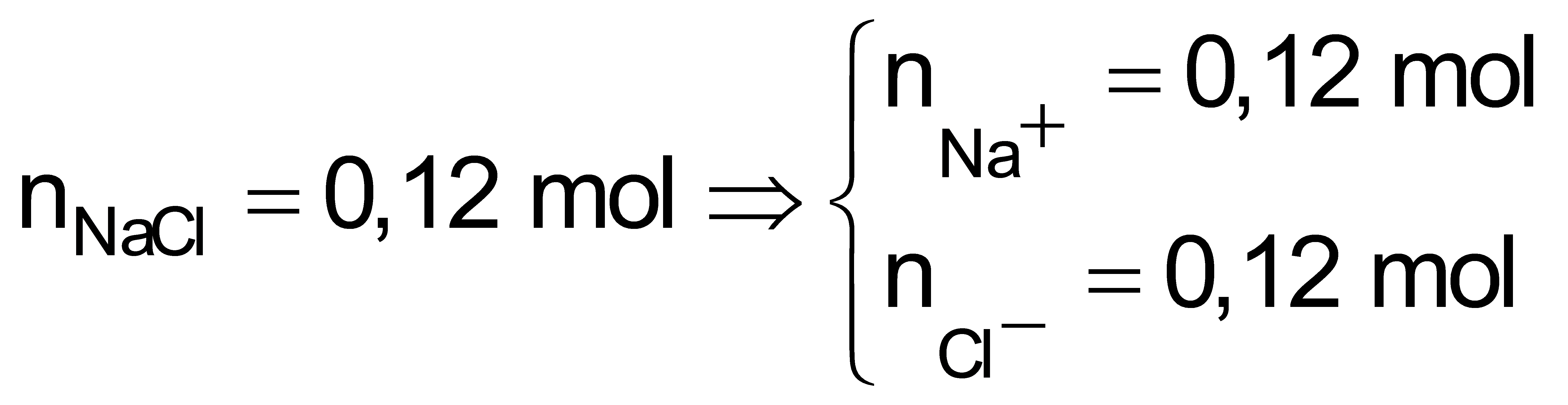 Các quá trình có thể xảy ra tại các điện cực:
Các quá trình có thể xảy ra tại các điện cực: 

![]() điện phân chưa hết
điện phân chưa hết ![]() H2O không bị điện phân
H2O không bị điện phân ![]() điện phân hết, H2O bị điện phân Các quá trình xảy ra tại các điện cực:
điện phân hết, H2O bị điện phân Các quá trình xảy ra tại các điện cực: 
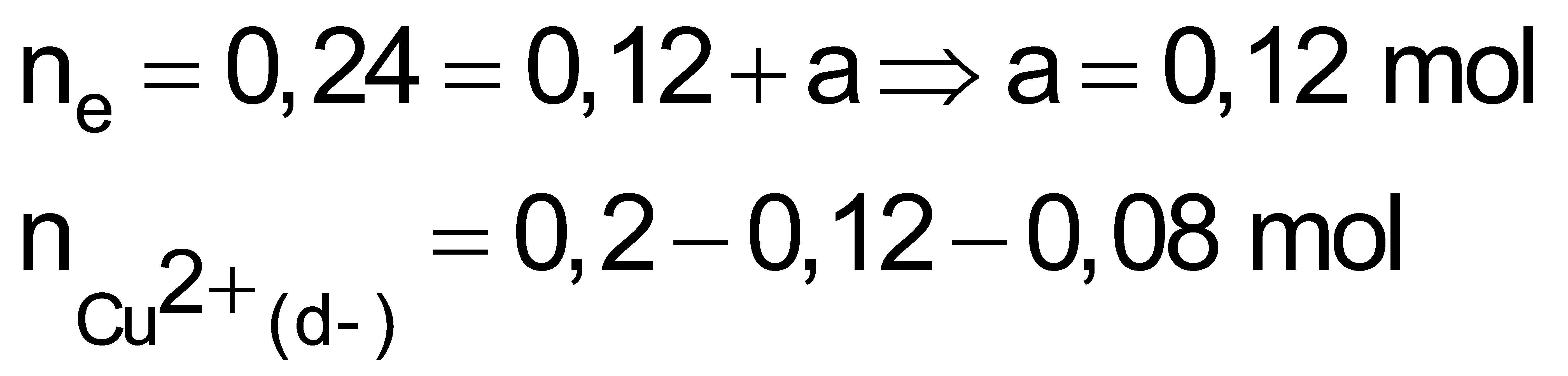
Dung dịch sau điện phân gồm Cu2+ :0,08 mol; H+ 0,12 mol; Na+ và SO42-. Dung dịch sau phản ứng tác dụng với thanh Mg. Các phương trình hóa học:
Mg + Cu2+ ![]() Mg2+ + Cu
Mg2+ + Cu
Mg + 2H+ ![]() Mg2+ + H2
Mg2+ + H2 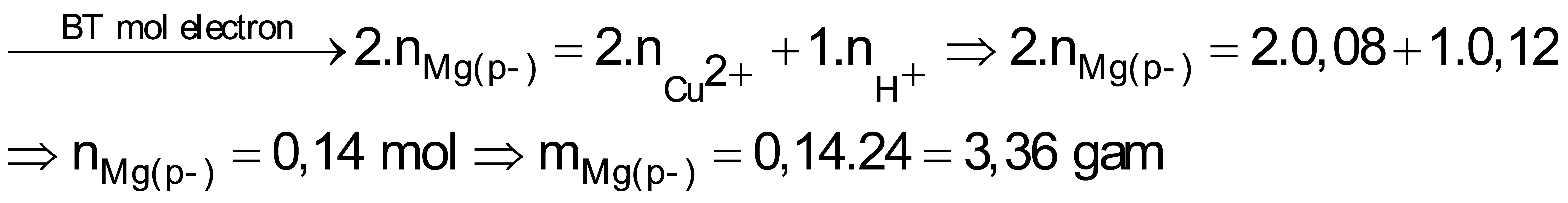
![]()
![]() Khối lượng thanh magie tăng:
Khối lượng thanh magie tăng: ![]()
Vậy đáp án đúng là C.

 không phụ thuộc vào
không phụ thuộc vào  ta có
ta có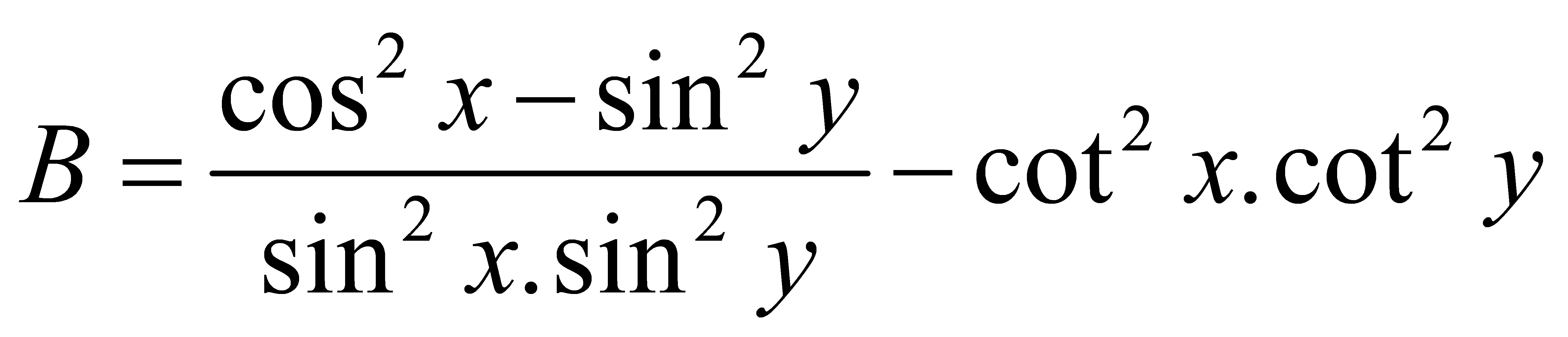 không phụ thuộc vào
không phụ thuộc vào