Đốt cháy hoàn toàn 4,4 gam sunfua của kim loại M (công thức MS) trong oxi dư. Chất rắn sau phản ứng đem hòa tan trong một lượng vừa đủ dung dịch HNO3 37,8% thấy nồng độ % của muối trong dung dịch là 4,72%. Khi làm lạnh dung dịch này thì thoát ra 8,08 gam muối rắn. Lọc tách muối rắn thấy nồng độ % của muối trong dung dịch là 34,7%. Công thức muối rắn tách ra sau phản ứng là:
A: Fe(NO3)2.9H2O
B: Cu(NO3)2.5H2O
C: Fe(NO3)2.9H2O
D: A,B,C đều sai.
Chọn C Khối lượng mol của Fe(NO3)2.9H2O; Cu(NO3)2.5H2O và Fe(NO3)3.9H2O lần lượt là 342, 278, 404 Ta có m muối rắn = 8,08g, chia cho khối lượng mol của 3 muối Chỉ có số mol Fe(NO3)3.9H2O là chẵn và bằng 0,02 mol, ta sẽ thử chọn C Từ C suy ra MS của FeS, nFeS = 0,05 mol Þ chất rắn là Fe2O3, ![]() = 0,025 mol Þ
= 0,025 mol Þ ![]() = 4g Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
= 4g Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O ![]() Þ mdung dịch
Þ mdung dịch ![]() =
= 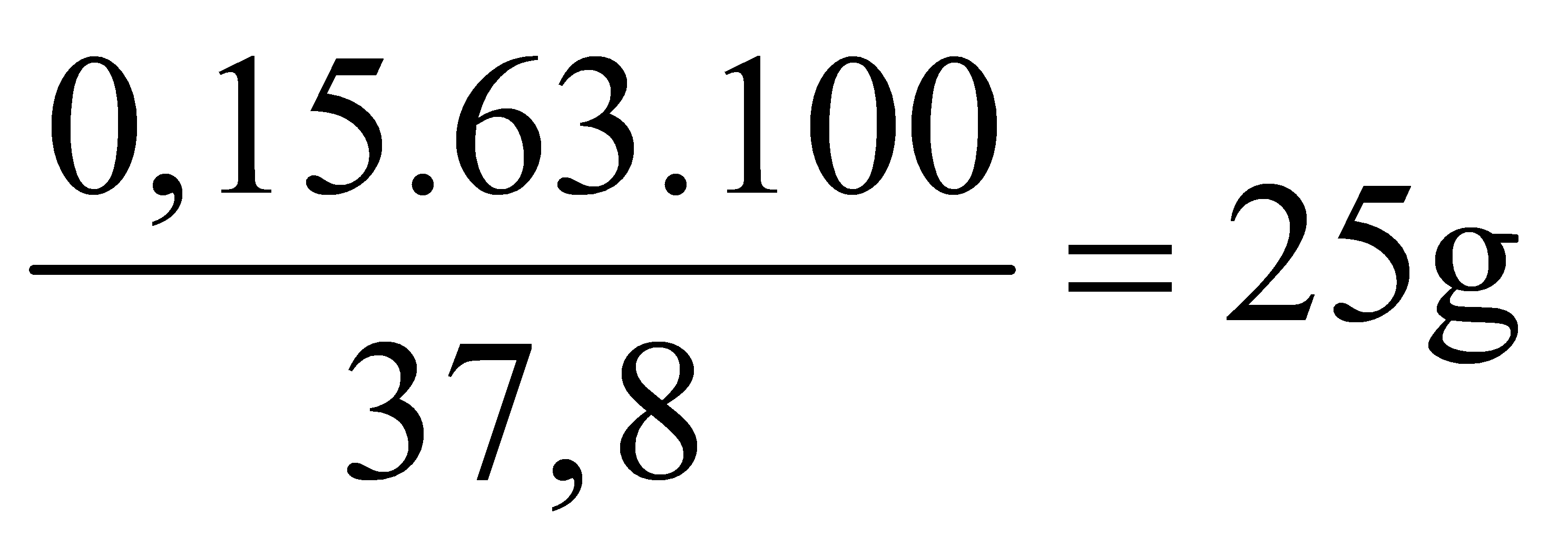 Sau khi làm lạnh ta có
Sau khi làm lạnh ta có ![]() còn lại: = 0,05 - 0,02 = 0,03 mol Þ
còn lại: = 0,05 - 0,02 = 0,03 mol Þ ![]() còn lại = 7,26 g mdd còn lại = 25+4-8,08 = 20,92 g Þ
còn lại = 7,26 g mdd còn lại = 25+4-8,08 = 20,92 g Þ ![]() còn lại =
còn lại = 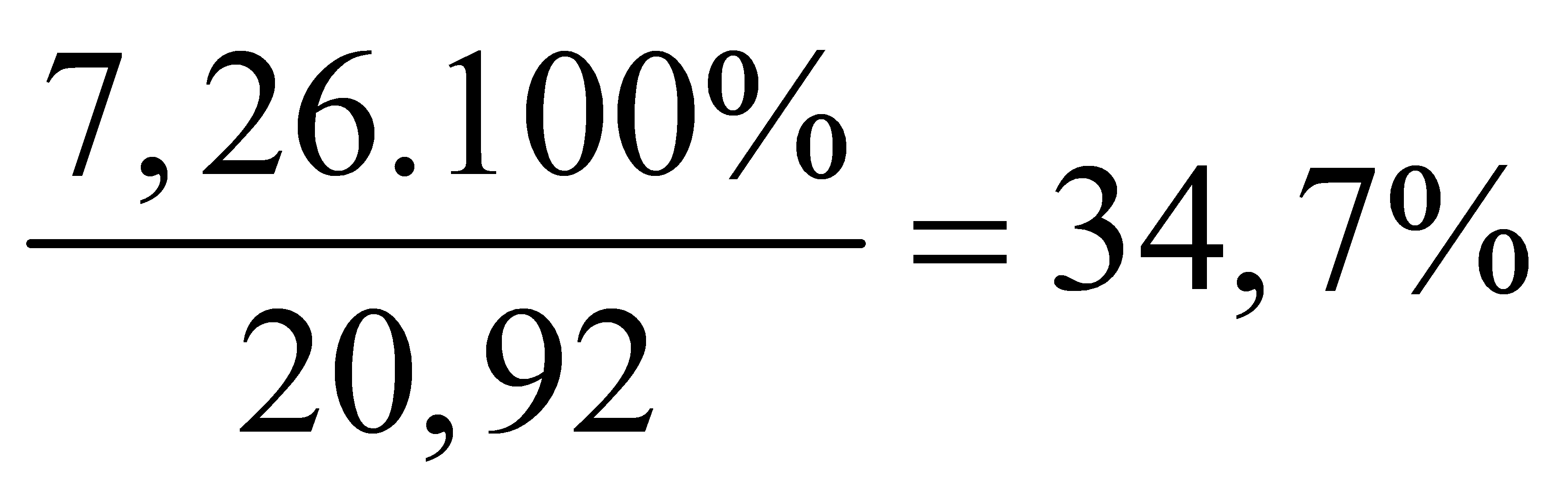 Þ Thỏa mãn.
Þ Thỏa mãn.
VẬY ĐÁP ÁN LÀ C

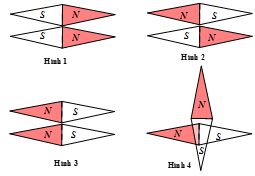 cân bằng, hướng của hai kim nam châm đó sẽ có dạng như hình
cân bằng, hướng của hai kim nam châm đó sẽ có dạng như hình