Hòa tan 64,258 gam hỗn hợp rắn gồm Cu(NO3)2.5H2O và NaCl vào nước được dung dịch X. Điện phân X với cường độ dòng điện không đổi, sau một thời gian thì thu được dung dịch Y có khối lượng giảm đi 18,79 gam so với dung dịch X. Cho 10 gam Fe vào dung dịch Y đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn T gồm 2 kim loại, đồng thời thoát ra 1,568 lít hỗn hợp Z gồm 2 khí màu nâu đỏ (đktc), màu nâu đậm dần trong không khí, tỉ khối hơi của Z so với H2 là 129/7. Giá trị của m là:
5,928.
6,142.
4,886.
5,324.
Hỗn hợp Z gồm hai khí có màu nâu đỏ, màu nâu đậm dần trong không khí ![]() Z gồm NO, NO2:
Z gồm NO, NO2: 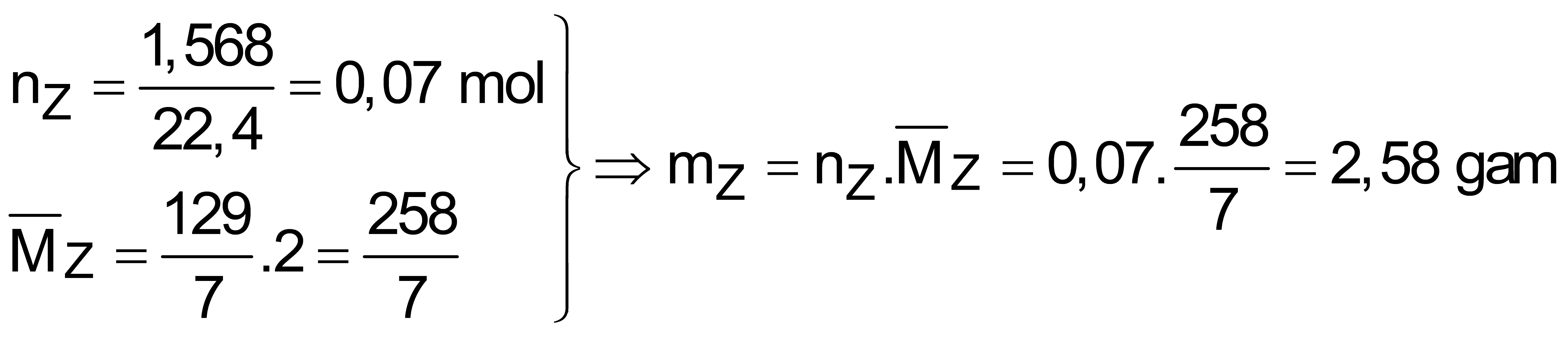
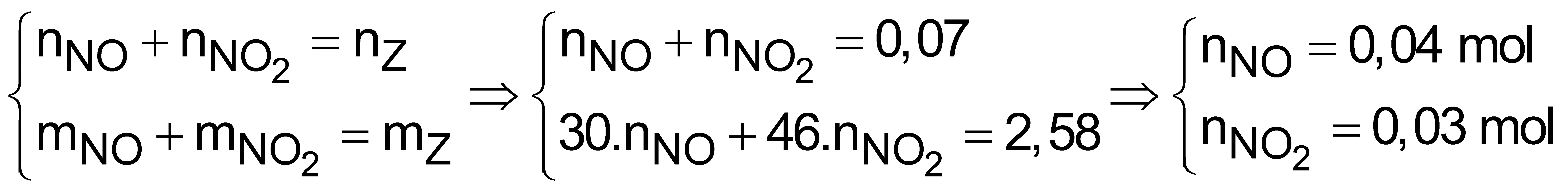 Cho E vào dung dịch Y thu được hai kim loại và khí NO, NO2
Cho E vào dung dịch Y thu được hai kim loại và khí NO, NO2 ![]() Dung dịch Y có
Dung dịch Y có ![]() Các quá trình tham gia của
Các quá trình tham gia của ![]() :
: 
![]() *Xét quá trình tham gia điện phân dung dịch X: Đặt số mol các chất Cu(NO3)2.5H2O: a mol; NaCl: b mol
*Xét quá trình tham gia điện phân dung dịch X: Đặt số mol các chất Cu(NO3)2.5H2O: a mol; NaCl: b mol ![]() Dung dịch X gồm
Dung dịch X gồm ![]() và
và ![]() Các quá trình xảy ra ở các điện cực:
Các quá trình xảy ra ở các điện cực: 

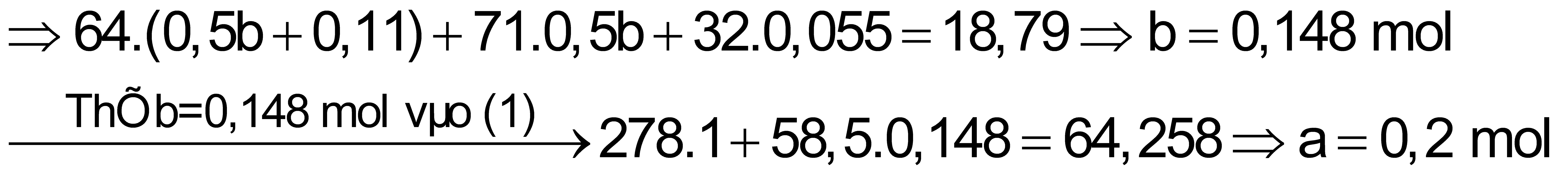
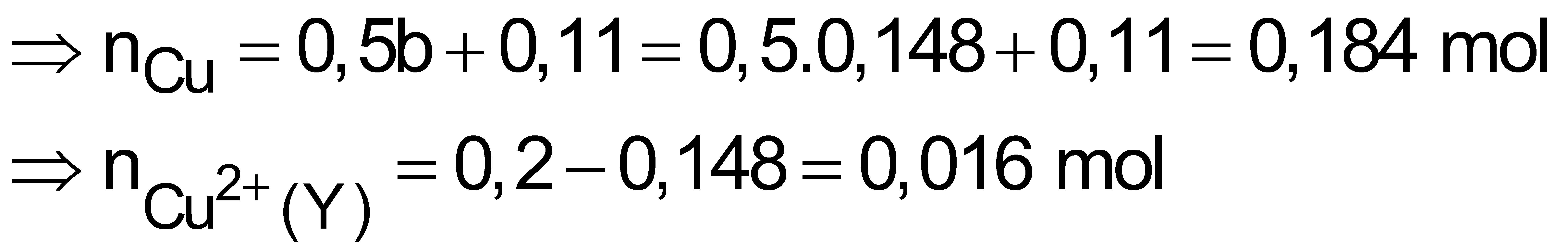 Xét giai đoạn Fe tác dụng với dung dịch Y: Dung dịch Y gồm
Xét giai đoạn Fe tác dụng với dung dịch Y: Dung dịch Y gồm ![]() và
và ![]() T gồm hai kim loại
T gồm hai kim loại ![]() T gồm Cu và Fe dư
T gồm Cu và Fe dư ![]() Fe bị oxi hóa lên Fe(II)
Fe bị oxi hóa lên Fe(II) 
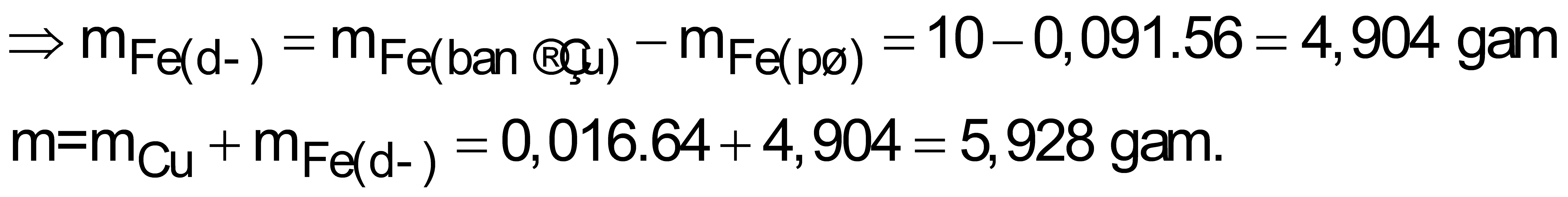
Vậy đáp án đúng là A.
