Hòa tan hết 8,72 gam hỗn hợp FeS2, FeS và Cu vào 400 ml dung dịch HNO3 4M, sản phẩm thu được gồm dung dịch X và một chất khí thoát ra. Nếu cho dung dịch BaCl2 dư vào dung dịch X thì thu được 27,96 gam kết tủa, còn nếu cho dung dịch Ba(OH)2 dư vào dung dịch X thì thu được 36,92 gam kết tủa. Mặt khác, dung dịch X có khả năng hòa tan tối đa m gam Cu. Biết trong các quá trình trên, sản phẩm khử duy nhất của 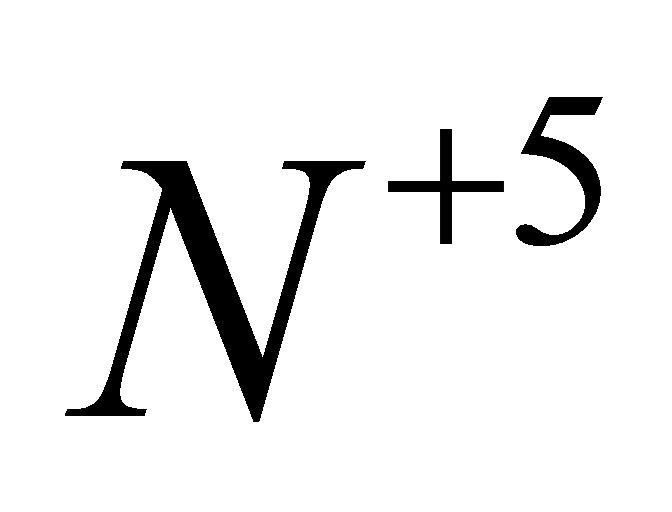 đều là NO. Giá trị của m là ?
đều là NO. Giá trị của m là ?
32,96.
9,92.
30,72.
15,68.
Phương pháp : Qui đổi, Bảo toàn e, Bảo toàn điện tích, Bảo toàn nguyên tố.
B1 : Xác định số mol các chất trong X. Qui đổi hỗn hợp đầu thành Fe, Cu , S. Khi X phản ứng với BaCl2 dư thì : ![]() Gọi a và b lần lượt là số mol của Fe và Cu. => 56a + 64b + 32.0,12 = 8,72g(1) Khi cho Ba(OH)2 dư thì kết tủa gồm Fe(OH)3; Cu(OH)2 ; BaSO4 => m kết tủa = 107a + 98b + 27,96 = 36,92(2)
Gọi a và b lần lượt là số mol của Fe và Cu. => 56a + 64b + 32.0,12 = 8,72g(1) Khi cho Ba(OH)2 dư thì kết tủa gồm Fe(OH)3; Cu(OH)2 ; BaSO4 => m kết tủa = 107a + 98b + 27,96 = 36,92(2)
Từ (1), (2) => a = 0,07 ; b = 0,015 moi
B2: Xác định các ion trong dung dịch X. Bảo toàn e : ![]() =>
=> ![]() dư =
dư = ![]()
Trong dung dịch X, Bảo toàn điện tích : ![]()
![]()
B3: Tính lượng Cu phản ứng Khi cho Cu vào thì Cu bị hòa tan bởi : ![]()
![]()
![]() pứ
pứ 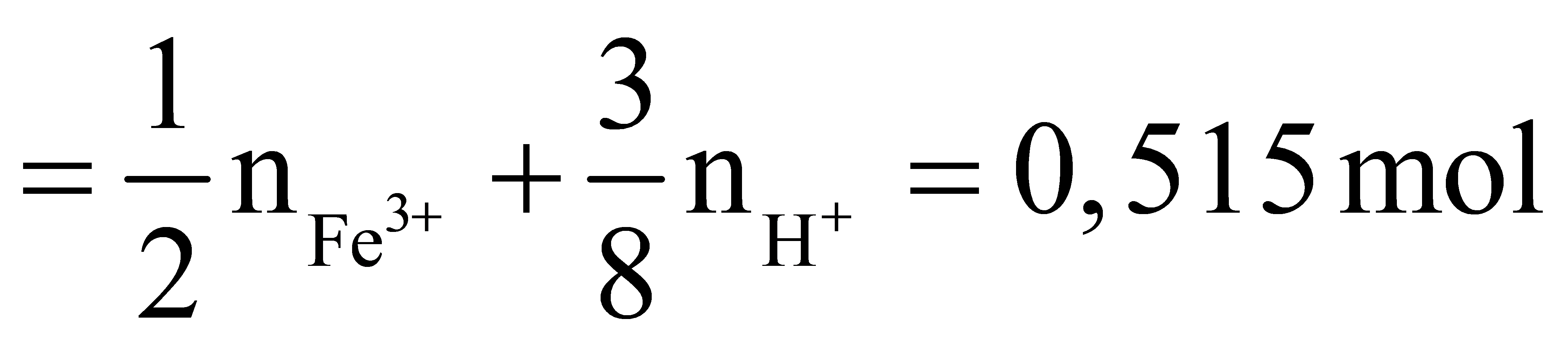
![]()
Vậy đáp án đúng là A

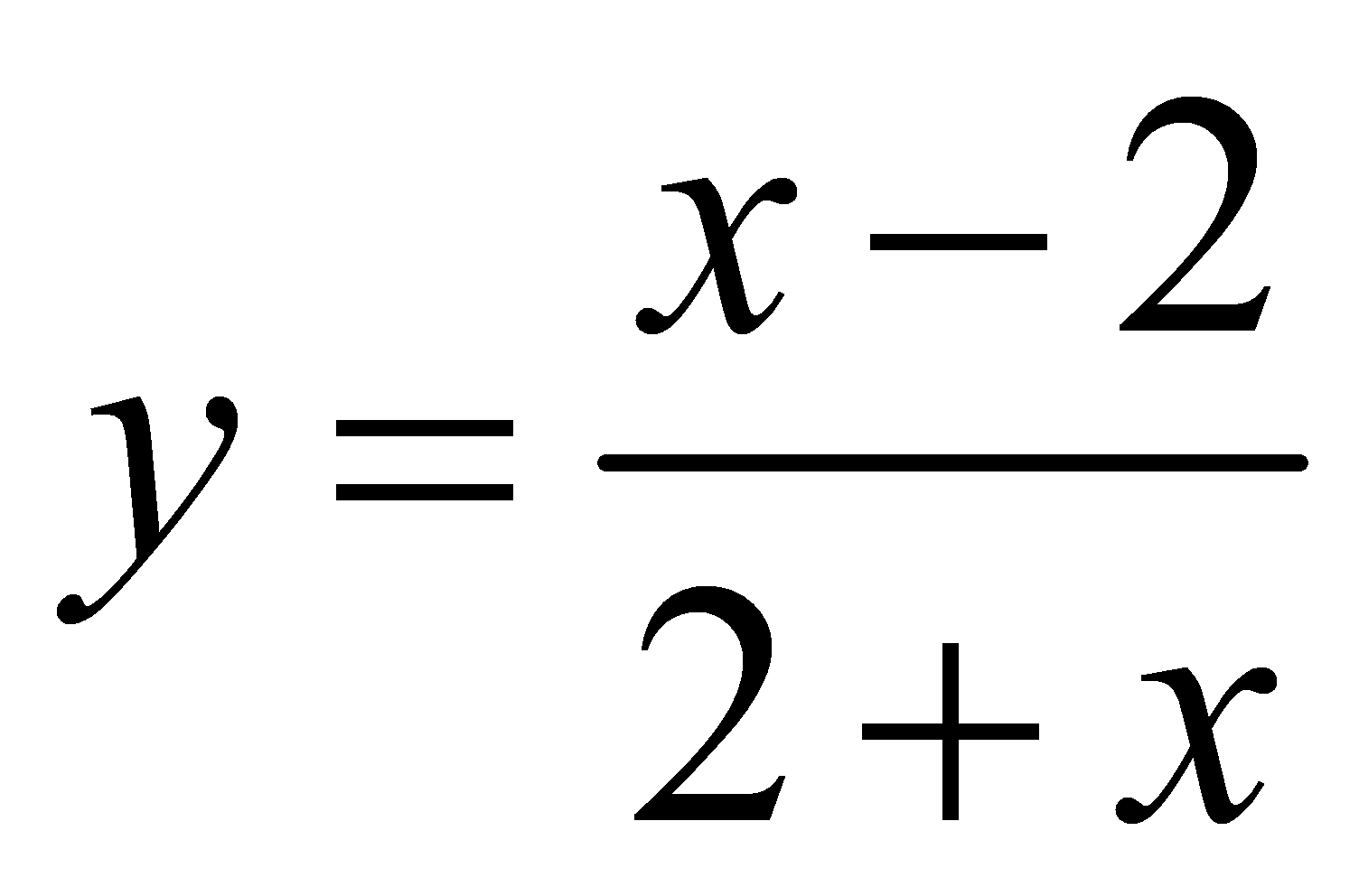 là
là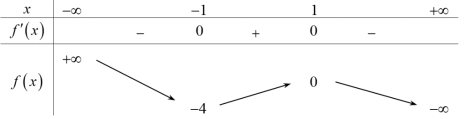
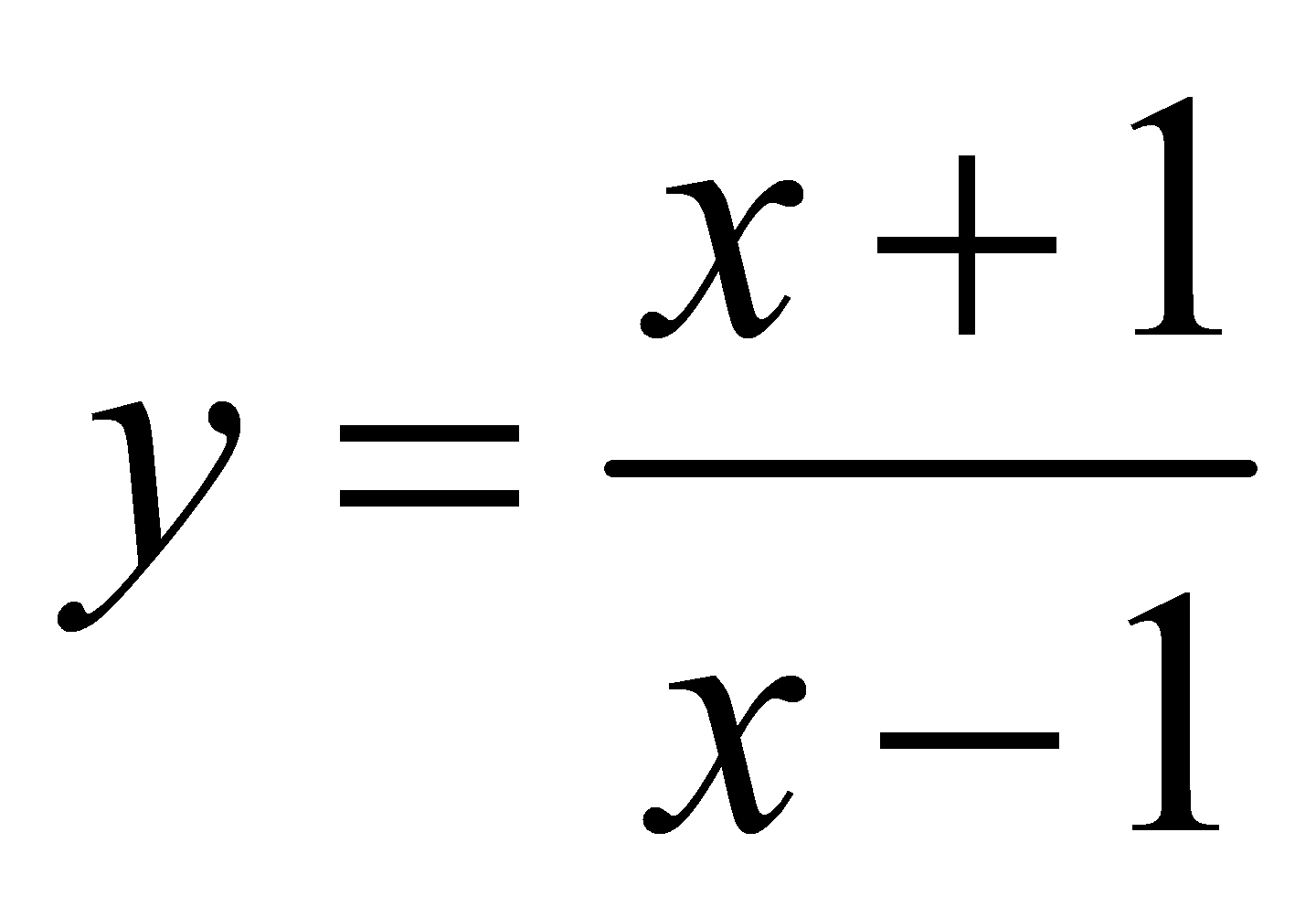 có đồ thị
có đồ thị