Hoà tan hoàn toàn 6,15 (gam) hỗn hợp X gồm 2 kim loại Na và M (hoá trị n không đổi) trong nước thu được dung dịch Y và 5,04 (lít) khí H2 (đktc). Để trung hoà 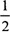 dung dịch Y cần dùng 25 (ml) dung dịch HCl 1M. Kim loại M là:
dung dịch Y cần dùng 25 (ml) dung dịch HCl 1M. Kim loại M là:
Ca.
Al.
Be.
Mg.
Al.
23x + M.y = 6,15 (1)
X + H2O:
2Na + 2H2O ![]() 2Na+ + 2OH− + H2↑ (2)
2Na+ + 2OH− + H2↑ (2)
x x x/2
- Nếu M tác dụng trực tiếp với nước:
2M + nH2O ![]() 2Mn+ + 2nOH− + nH2↑ (3)
2Mn+ + 2nOH− + nH2↑ (3)
y ny ny/2
- Nếu M là kim loại có hiđroxit lưỡng tính:
M + (4−n)OH− + (n−2)H2O ![]()
![]() + n/2H2↑ (4)
+ n/2H2↑ (4)
y (4−n)y ny/2
TH1: (3) xảy ra → từ (2) và (3) ![]()
![]() = x/2 + ny/2 =
= x/2 + ny/2 = ![]() = 0,225 (mol).
= 0,225 (mol).
![]() x + ny = 0,45 (5)
x + ny = 0,45 (5)
Dung dịch Y chứa OH−: (x + ny) mol
![]() Y + dd HCl:
Y + dd HCl:
OH− + H+ ![]() H2O
H2O
![]() (x + ny)
(x + ny) ![]() (x + ny)
(x + ny)
(5) ![]() nH+ =
nH+ = ![]() (x + ny) = 0,025
(x + ny) = 0,025 ![]() x + ny = 0,05 < 0,45 (Loại).
x + ny = 0,05 < 0,45 (Loại).
TH2: (4) xảy ra, do OH− dư nên M tan hết → từ (2) và (4) ![]() x + ny = 0,45 (6)
x + ny = 0,45 (6)
nH+ = ![]() nOH− dư (4) =
nOH− dư (4) = ![]() (x − (4 − n)y) = 0,025
(x − (4 − n)y) = 0,025 ![]() x +(4 − n)y = 0,05 (7)
x +(4 − n)y = 0,05 (7)
Từ (1), (5) và (7) ![]() M = 9n
M = 9n ![]() n = 3 và M = 27 (Al).
n = 3 và M = 27 (Al).

 . Hỏi hàm số
. Hỏi hàm số 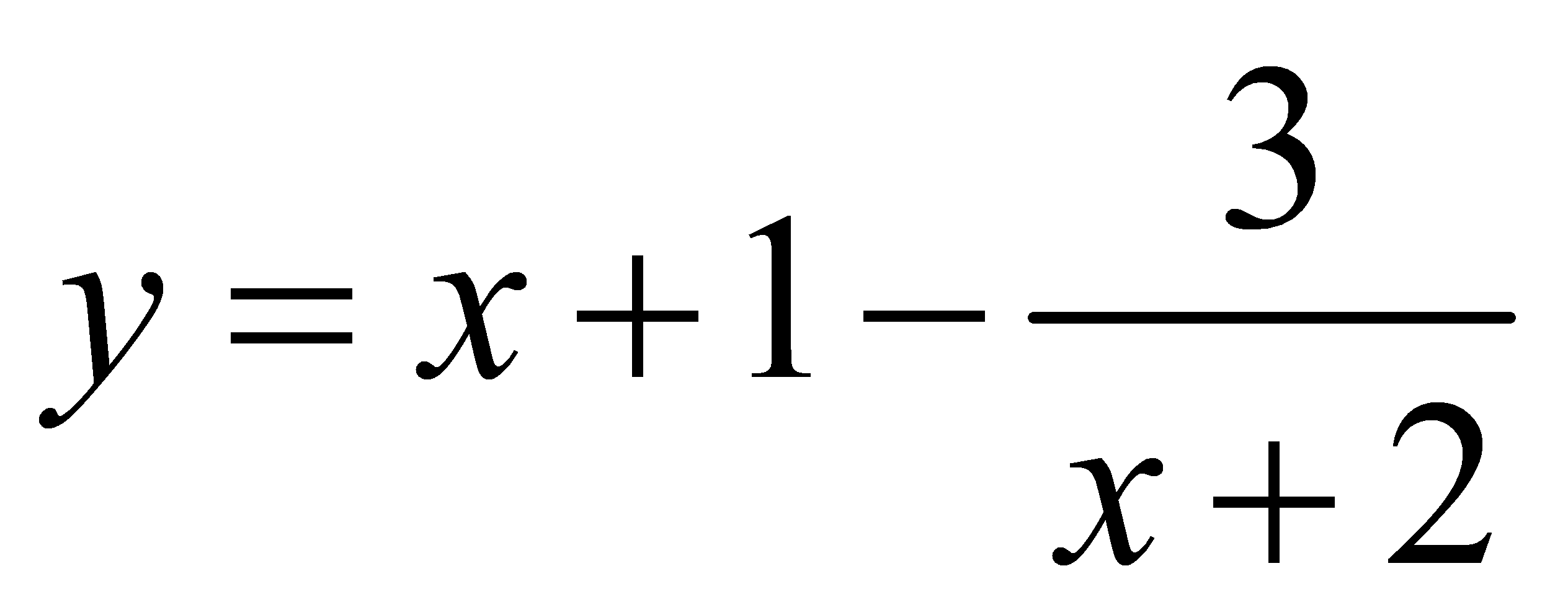 trên đoạn
trên đoạn  đạt cực tiểu tại x bằng:
đạt cực tiểu tại x bằng: