Hòa tan hỗn hợp chứa 0,15 mol Mg và 0,15 mol Al vào dung dịch hỗn hợp chứa 0,15 mol Cu(NO3)2 và 0,525 mol AgNO3. Khi phản ứng xảy ra hoàn toàn khối lượng chất rắn thu được là:
32,4 gam.
56,7 gam.
63,9 gam.
66,3 gam.
63,9 gam.
Tính oxi hóa: Ag+ > Cu2+ ![]() Ag+ bị khử trước Cu2+.
Ag+ bị khử trước Cu2+.
Tính khử: Mg > Al ![]() Mg bị oxi hóa trước Al.
Mg bị oxi hóa trước Al.
Phản ứng xảy ra theo thứ tự:
Mg + 2Ag+ ![]() Mg2+ + 2Ag↓ (1)
Mg2+ + 2Ag↓ (1)
0,15 → 2.0,15 → 0,15
nAg+ dư = 0,525 − 0,3 = 0,225 (mol).
Al + 3Ag+ ![]() Al3+ + 3Ag↓ (2)
Al3+ + 3Ag↓ (2)
0,075 ← 0,225 → 0,225
nAl dư = 0,15 − 0,075 = 0,075 (mol).
2Al + 3Cu2+ ![]() 2Al3+ + 3Cu↓ (3)
2Al3+ + 3Cu↓ (3)
0,075 → 0,1125 → 0,1125
nCu2+ dư = 0,15 − 0,1125 = 0,0375 (mol).
Từ (1), (2) và (3) 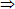 mCR = 108.0,525 + 64.0,1125 = 63,9 gam.
mCR = 108.0,525 + 64.0,1125 = 63,9 gam.

 AlCl3
AlCl3