Nitro hóa benzen bằng HNO3 thu được hai chất hữu cơ A, B (hơn kém nhau một nhóm -NO2). Khi đốt cháy hoàn toàn 2,34 (gam) hỗn hợp A, B tạo thành CO2, H2O và 255,8 (ml) N2 (27°C và 740 mm Hg). Vậy A, B lần lượt là:
Nitrobenzen và 1,3-đinitrobenzen.
Nitrobenzen và 1,3,5-trinitrobenzen.
1,3-đinitrobenzen và 1,3,5-trinitrobenzen.
Nitrobenzen và 1,4-đinitrobenzen.
Nitrobenzen và 1,3 - đinitrobenzen.
Trung bình mỗi phân tử C6H6 phản ứng với k phân tử HNO3
C6H6 + kHNO3 → C6H6-k(NO2)k + kH2O
Đốt cháy hỗn hợp A và B thu được nN2 = 0,2558.(740/760)/(0,082.300) = 0,01(mol)
Số mol HNO3 phản ứng: nHNO3 = 2.nN2 = 2.0,01 = 0,02(mol)
nH2O = nHNO3 = 0,02 mol
Bảo toàn khối lượng:
mC6H6 + mHNO3 = m(hh) + mH2O
⇒ mC6H6 + 63.0,02 = 2,34 + 18.0,02
⇒ mC6H6 = 1,44g
nC6H6 = 1,44/78 = 6/325(mol)
k = nHNO3/nC6H6 =13/12
Hai sản phẩm A, B hơn kém nhau một nhóm −NO2 nên một chất có một nhóm −NO2, chất kia có hai nhóm −NO2
Nhóm −NO2 hút điện tử nên nhóm −NO2 còn lại vào vị trí metanzen...
Vậy 2 chất cần tìm là: Nitrobenzen và 1,3 - đinitrobenzen.


 với
với 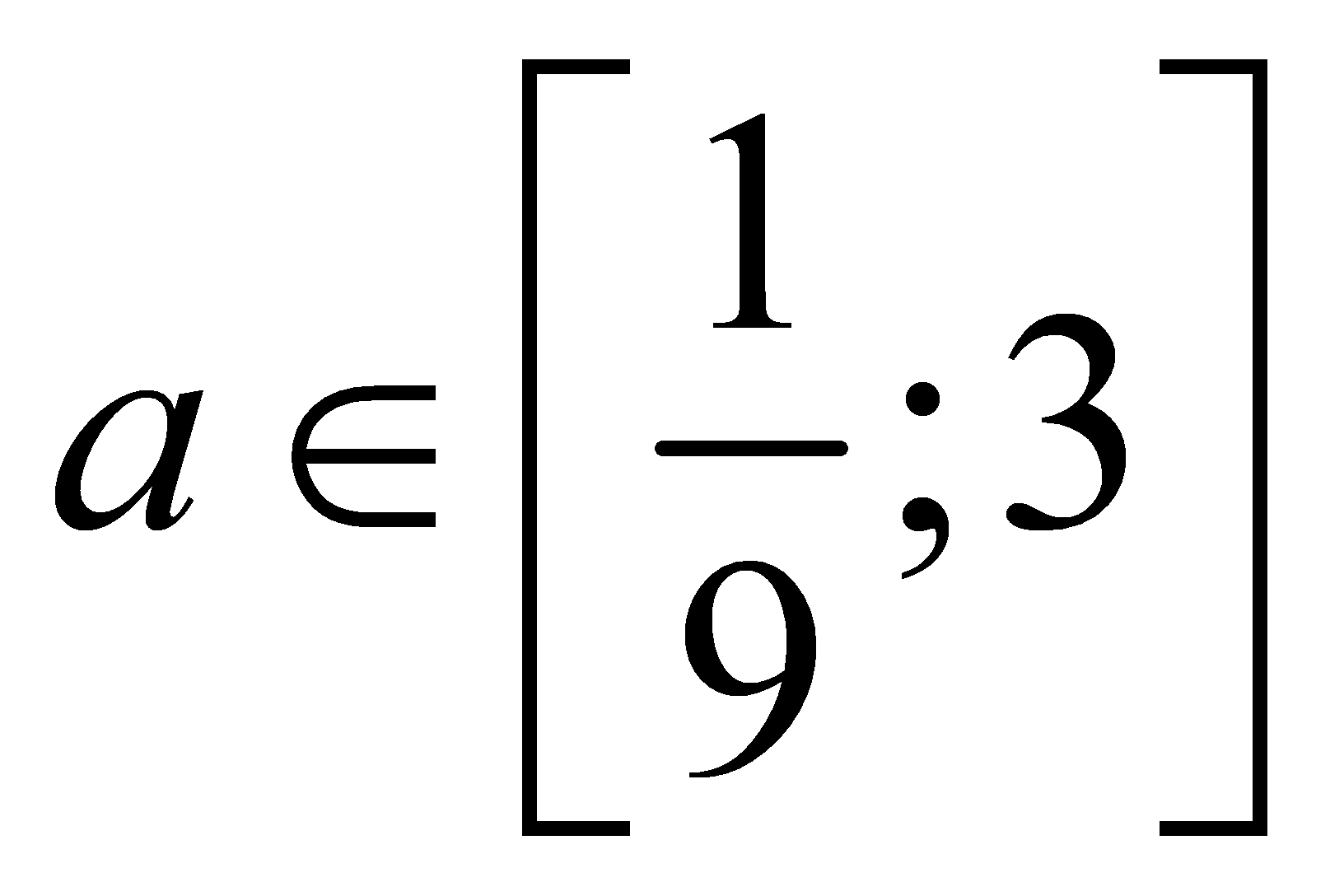 và M, m lần lượt là giá trị lớn nhất và giá trị nhỏ nhất của biểu thức P. Khi đó giá trị của
và M, m lần lượt là giá trị lớn nhất và giá trị nhỏ nhất của biểu thức P. Khi đó giá trị của