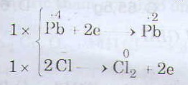Nội dung bài giảng
Cân bằng phương trình hóa học của các phản ứng oxi hóa – khử sau bằng các phương pháp thăng bằng electron :
a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
b) HNO3 + HCl → NO + Cl2 + H2O
c) HClO3 + HCl → Cl2 + H2O
d) PbO2 + HCl → PbCl2 + Cl2 + H2O
Hướng dẫn giải:
Cân bằng phương trình hóa học của các phản ứng oxi hóa – khử sau bằng các phương pháp thăng bằng electron:
a) 2\(\overset{+7}{KMnO_{4}}\)+ 16\(\overset{-1}{HCl}\)→ 2KCl + 2\(\overset{+2}{MnCl_{2}}\) + 5\(\overset{0}{Cl_{2}}\) + 8H2O

b) \(6\overset{-1}{HCl}\) + \(2\overset{+5}{HNO_{3}}\) → \(2\overset{+2}{NO}\) + 3\(\overset{0}{Cl_{2}}\) +4 H2O

c) 5\(\overset{-1}{HCl}\) + \(\overset{+5}{HClO_{3}}\) → 3\(\overset{0}{Cl_{2}}\)+ 3H2O

d) \(\overset{+4}{PbO_{2}}\) + 4\(\overset{-1}{HCl}\) → \(\overset{+2}{PbCl_{2}}\)+\(\overset{0}{Cl_{2}}\) + 2H2O