Cho 46,8 gam hỗn hợp CuO và Fe3O4 (tỉ lệ mol 1:1) tan hết trong dung dịch H2SO4 loãng, vừa đủ, thu được dung dịch A. Cho m gam Mg vào A, sau khi phản ứng kết thúc thu được dung dịch B. Thêm dung dịch KOH dư vào B được kết tủa D. Nung D trong không khí đến khối lượng không đổi, thu được 45,0 gam chất rắn E. Giá trị gần nhất của m là ?
6,6.
11,0.
13,2.
8,8.
Gọi số mol của CuO và và Fe3O4 lần lượt là x, x mol
→ 80x + 232 x = 46,8 → x = 0,15 mol
Hòa tan hỗn hợp trong H2SO4 vừa đủ thu được dung dịch A chứa : Fe2+ : 0,15 mol, Fe3+ : 0,3 mol, Cu2+ : 0,15 mol và SO42-Khi cho Mg vào dung dich A thì thứ tự Mg phản ứng là Fe3+, Cu2+, Fe2+
Nhận thấy nếu mE = 45 gam < mCuO + mFe2O3 = 0,15. 80 +![]() . 160 = 48 gam
. 160 = 48 gam
→ chứng tỏ Fe3+ đã phản ứng hết
TH1: Nếu có x mol Cu2+ tham gia phản ứng thì E chứa Fe2O3: 0,225 mol, CuO : (0,15-x) mol, MgO : (0,15 +x) mol( bảo toàn e)
→ 0,225. 160 + 80. ( 0,15-x ) + 40. ( 0,15 +x ) = 45 → x = 0,225 ( loại vì x > 0,15)
TH2: Nếu có x mol Fe2+ tham gia phản ứng thì E chứa CuO : 0,15 mol, Fe2O3: (0,225-0,5x), (MgO : 0,15+ 0,15 + x) mol ( bảo toàn e)
→ 0,15. 80 + 160. ( 0,225-0,5x) + 40. (0,15+ 0,15 +x) = 45
→ x = 0,075 mol→ m = 24. ( 0,075 + 0,15+ 0,15) = 9 gam.
Vậy đáp án đúng là D

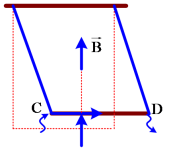 nhẹ, cách điện sao cho đoạn dây CD nằm ngang. Đưa đoạn dây đồng vào trong từ trường đều có cảm ứng từ
nhẹ, cách điện sao cho đoạn dây CD nằm ngang. Đưa đoạn dây đồng vào trong từ trường đều có cảm ứng từ