Cho 6,45 gam hỗn hợp bột X gồm hai kim loại Al và Mg có tỉ lệ mol tương ứng 3 : 2 vào 150 (ml) dung dịch Y chứa Fe(NO3)2 1M và Cu(NO3)2 1M, khuấy đều cho đến khi kết thúc phản ứng thu được m gam chất rắn và dung dịch Z. Giá trị của m là:
12,90.
21,90.
19,20.
18,45.
18,45.
nAl = 3.![]() = 0,15 (mol)
= 0,15 (mol) 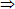 nMg = 0,1 (mol); nFe2+ = nCu2+ = 0,15 (mol).
nMg = 0,1 (mol); nFe2+ = nCu2+ = 0,15 (mol).
Tính oxi hóa: Cu2+ > Fe2+ 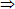 Cu2+ bị khử trước Fe2+.
Cu2+ bị khử trước Fe2+.
Tính khử: Mg > Al 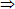 Mg bị oxi hóa trước Al.
Mg bị oxi hóa trước Al.
Phản ứng xảy ra theo thứ tự:
Mg + Cu2+ ![]() Mg2+ + Cu (1)
Mg2+ + Cu (1)
0,1 → 0,1 0,1
nCu2+ dư = 0,05 (mol).
2Al + 3Cu2+ ![]() 2Al3+ + 3Cu↓ (2)
2Al3+ + 3Cu↓ (2)
![]() ← 0,05 → 0,05
← 0,05 → 0,05
nAl dư = 0,15 − ![]() = 0,35/3 (mol).
= 0,35/3 (mol).
2Al + 3Fe2+ ![]() 2Al3+ + 3Fe↓ (3)
2Al3+ + 3Fe↓ (3)
0,1 ← 0,15 → 0,15
nAl dư = ![]() − 0,1 =
− 0,1 = ![]() (mol).
(mol).
Từ (1), (2) và (3) 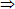 m = 64.0,15 + 56.0,15 + 27.
m = 64.0,15 + 56.0,15 + 27.![]() = 18,45 (gam).
= 18,45 (gam).

 tìm các giá trị của
tìm các giá trị của