Cho hỗn hợp X gồm 2 kim loại Al và Ba. Tiến hành 2 thí nghiệm :
Thí nghiệm 1: Cho m gam X vào nước dư thu được 1,344 lít H2 (ở đktc)
Thí nghiệm 2: Cho 2m gam X vào dung dịch Ba(OH)2 dư thu được 20,832 lít H2 (ở đkct)
Giá trị của m là ?
9,155g.
11,850g.
2,055g.
10,155g.
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2
Thí nghiệm 1: Đặt nAl = x; nBa = y.
Ở thí nghiệm 2: Khi cho vào dung dịch Ba(OH)2 dư, cả Ba và Al đều tan hết, lượng khí sinh ra lớn gấp 15,5 lần thí nghiệm 1 ![]() ở thí nghiệm 1 chỉ có Ba tan hết, Al còn dư.
ở thí nghiệm 1 chỉ có Ba tan hết, Al còn dư.
Thí nghiệm 2: ![]()
![]() y=0,015 (mol) nAl = 2x; nBa =2 y = 0,03 (mol)
y=0,015 (mol) nAl = 2x; nBa =2 y = 0,03 (mol)  →m=0,3.27 + 0,015.137 = 10,155g.
→m=0,3.27 + 0,015.137 = 10,155g.
Chú ý: Khi cho kim loại kiềm, kiềm thổ vào nước thu được H2 có  Khi cho Al+ dung dịch
Khi cho Al+ dung dịch ![]() ta được
ta được 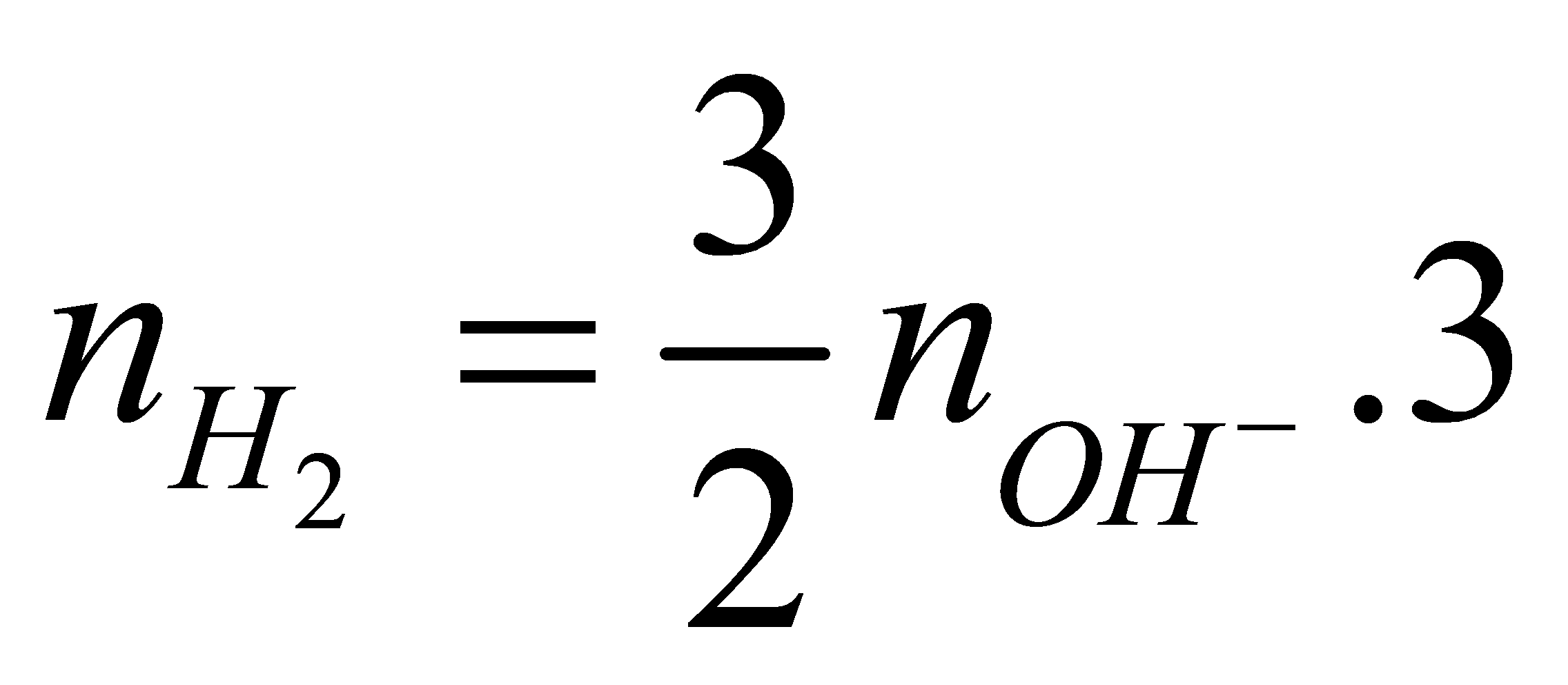
Vậy đáp án đúng là D
