Chu kỳ 3 của bảng tuần hoàn gồm các nguyên tố sắp xếp như sau:
Na
Mg
Al
Si
P
S
Cl
Ar
So sánh nào sau đây đúng?
A.A.
Bán kính nguyên tử: Na < Cl.
B.B.
Điện tích hạt nhân nguyên tử: Mg > P.
C.C.
Số lớp electron: Al < Ar.
D.D.
Bán kính ion: \(N{a^ + } < {S^{2 - }}\)
Đáp án và lời giải
Đáp án:D
Lời giải:
Chọn D.
Trong chu kỳ số lớp electron không đổi, điện tích hạt nhân tăng dần \( \to \) bán kính nguyên tử giảm dần.
Bán kính \(N{a^ + }\) nhỏ hơn \({S^{2 - }}\) vì nguyên nhân chính là \(N{a^ + }\) chỉ có 2 lớp electron, \({S^{2 - }}\) có 3 lớp electron.

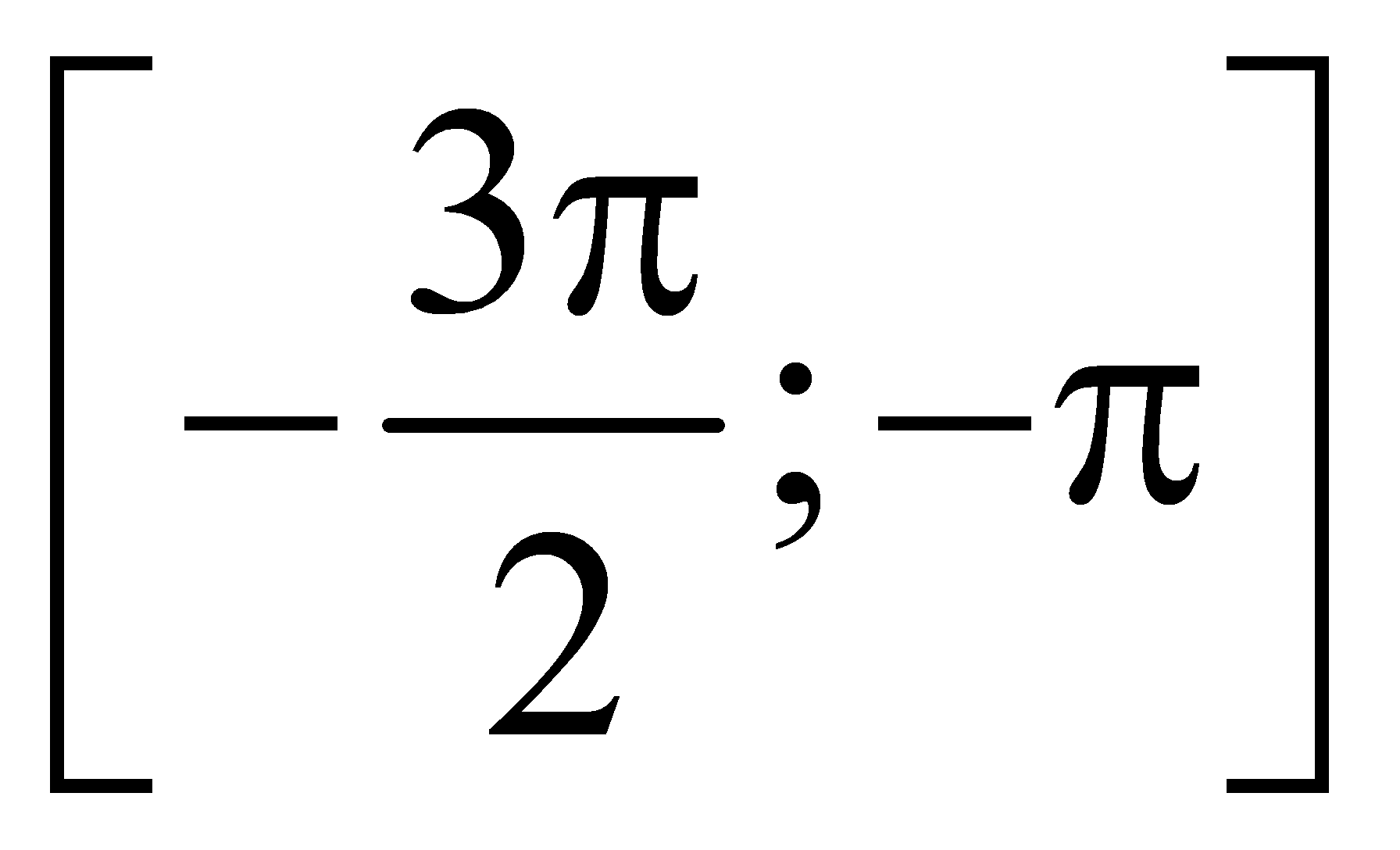 của phương trình
của phương trình 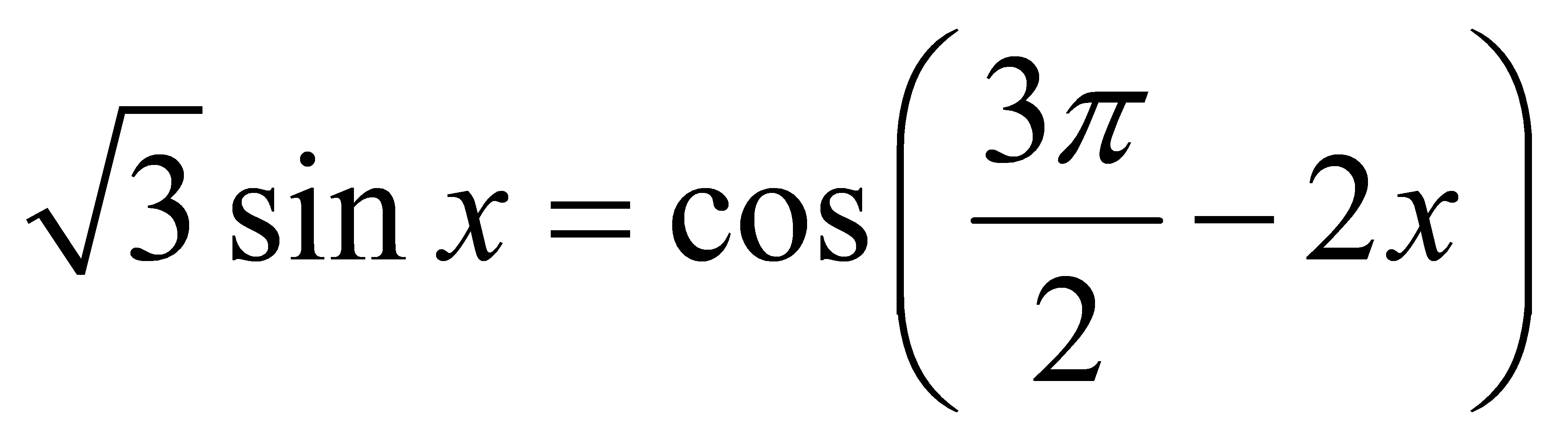 là:
là: