Điện phân 150 ml dung dịch AgNO3 1M với điện cực trơ trong t giờ, cường độ dòng điện không đổi 2,68A (hiệu suất quá trình điện phân là 100%), thu được chất rắn X, dung dịch Y và khí Z. Cho 12,6 gam Fe vào Y, sau khi các phản ứng xảy ra hoàn toàn, thu được 14,5 gam hỗn hợp kim loại và khí NO (sản phẩm khử duy nhất của N+5). Giá trị của t là:
0,6.
0,8.
1,0.
0,3.
Phân tích: xem dung dịch Y: bảo toàn 0,15 mol anion NO3-; Fe + Y → hỗn hợp kim loại + khí NO ||→ Y chứa cation Ag+ và H+.
Quan sát sơ đồ bài tập HNO3:
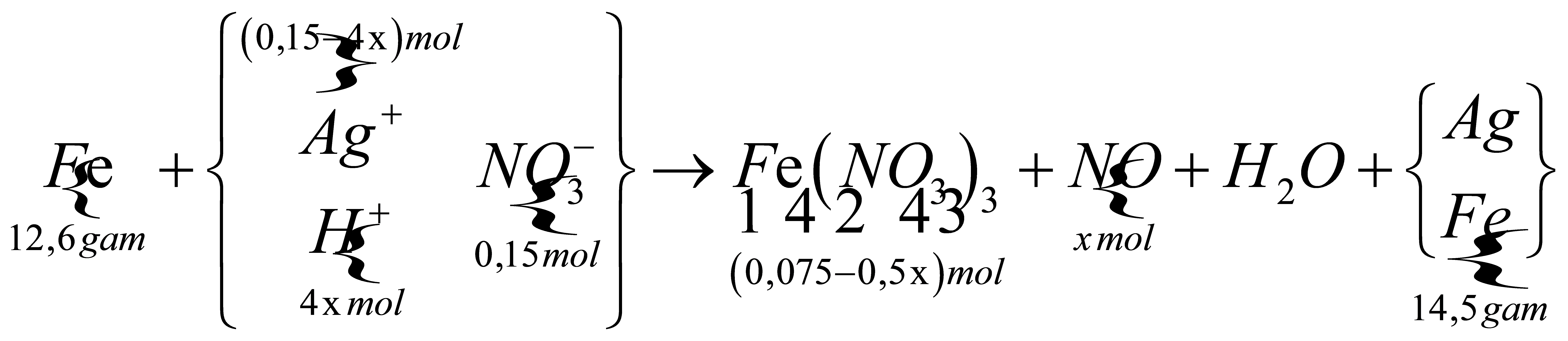
♦ BTKL kim loại: 12,6 + 108 × (0,15 – 4x) = 56 × (0,075 – ½.x) + 14,5
||→ x = 0,025 mol.
||→ ne trao đổi = nH+ sinh ra = 4z = 0,1 mol
||→ thời gian t = 96500 × 0,1 ÷ 2,68 = 3600 (s) ⇄ 1 giờ.
Vậy đáp án đúng là C.

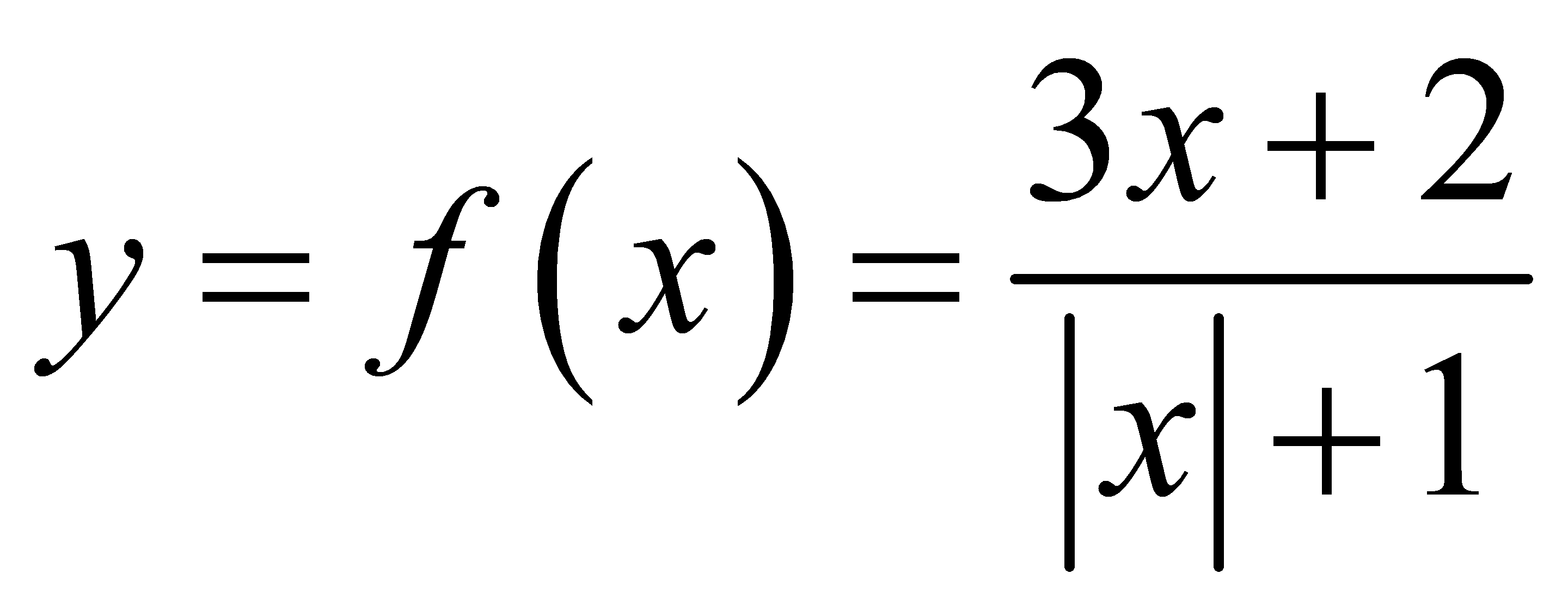 .
.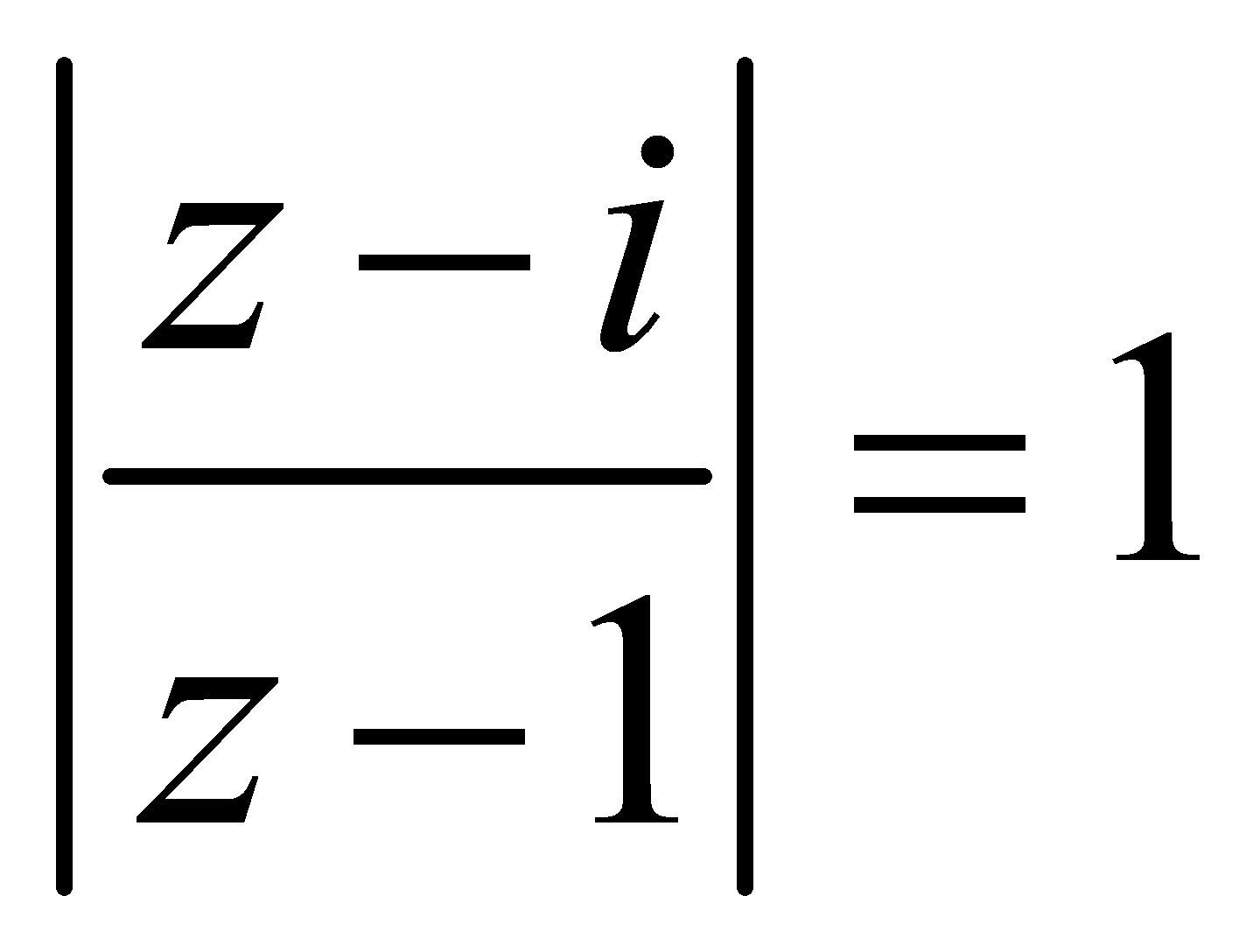 và
và 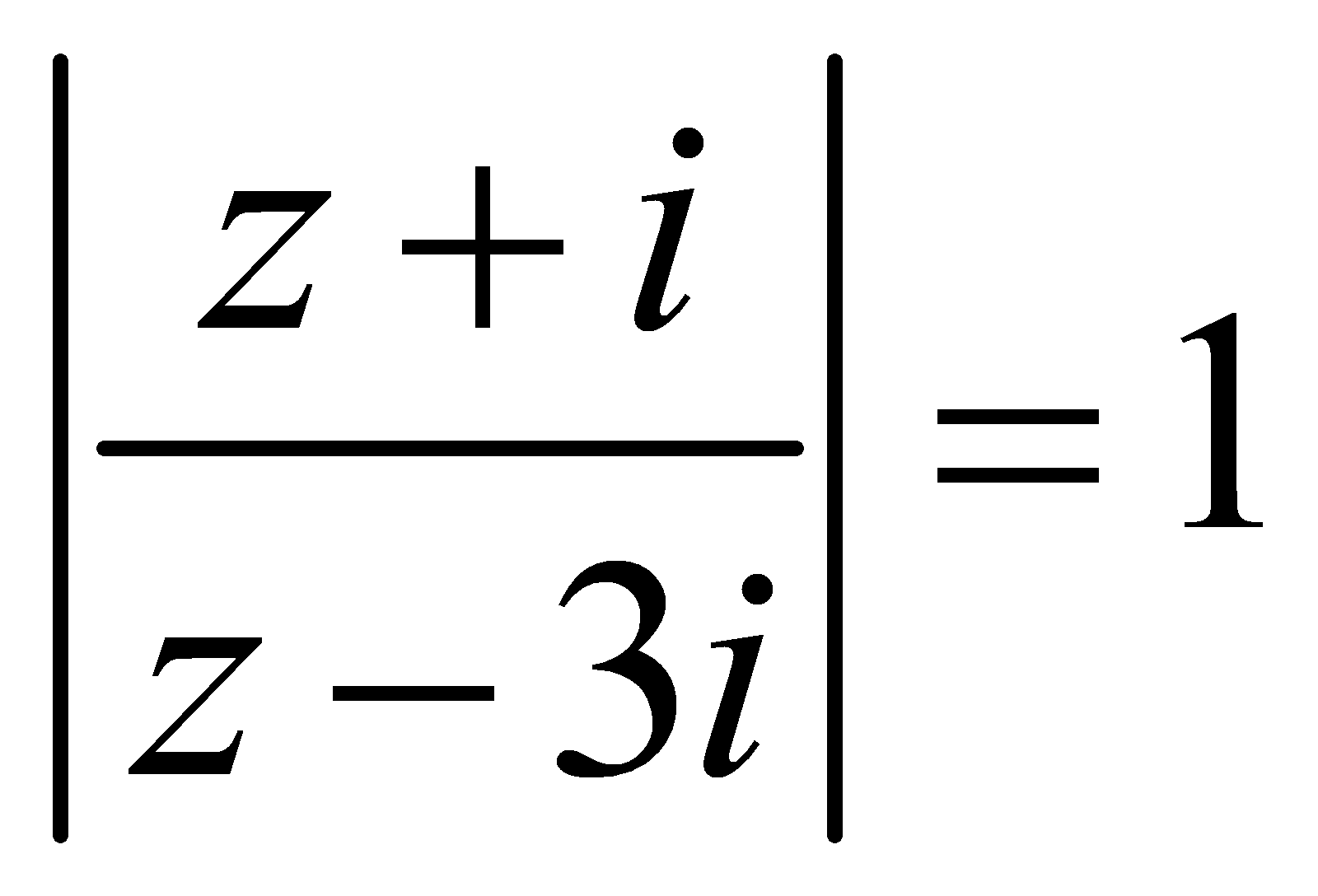 .
.