Điện phân dung dịch X chứa Cu(NO3)2 và NaCl với điện cực trơ thấy thể tích khí thoát ra ở cả 2 điện cực (V lít) và thời gian điện phân (t giây) phụ thuộc nhau như trên đồ thị.
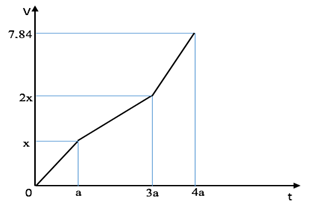
Nếu điện phân dung dịch trong thời gian 2,5a giây rồi cho dung dịch sau điện phân tác dụng với lượng Fe dư (NO là sản phẩm khử duy nhất của N+5) thì lượng Fe tối đa đã phản ứng là:

7,0.
4,2.
9,3.
6,1.
Phân tích:
Đoạn 1: Chỉ có Cl2 thoát ra.
Đoạn 2: Chỉ có O2 thoát ra.
Đoạn 3: Anot có O2 tiếp tục thoát ra. Catot có H2 thoát ra.
Trong đoạn 3 này thời gian bằng nửa đoạn 2 nên VO2 = 0,5x, bảo toàn electron =>VH2 = x
Tổng cộng 3 đoạn thì khí thoát ra gồm: Cl2 (x lít), O2 (1,5x lít) và H2 (x lít) => x + 1,5x + x = 7,84 => x = 2,24
Ban đầu: nNaCl = 2nCl2 = 0,2 mol
nCuSO4 = nCu = nCl2 + 2nO2 (đoạn 2) = 0,3
Tại thời điểm 2,5a giây (Thuộc đoạn 2) thì:
Anot: a giây đầu tạo Cl2,
1,5 giây còn lại O2: nCl2 = 0,1 và nO2 = 0,1.1.5/2 = 0,075mol
Bảo toàn electron => nCu (catot) = 0,25 => nCu2+ còn lại = 0,3 - 0,25 = 0,05 mol
nH+ = 4nO2 -> nNO = nH+/4 = 0,075 mol
Thêm Fe, bảo toàn electron: 2nFe = 2nCu2+ + 3nNO => nFe = 0,1625 mol
=> mFe = 9,1 gam.
Vậy đáp án đúng là D.

 là:
là: