Hòa tan hoàn toàn hỗn hợp X gồm Cu, CuO, Cu(NO3)2 (trong đó số mol Cu bằng số mol CuO) vào 350 ml dung dịch H2SO4 2M (loãng), thu được dung dịch X chỉ chứa một chất tan duy nhất, và có khí NO thoát ra. Phần trăm khối lượng Cu trong X có giá trị gần nhất với giá trị nào sau đây?
Đặt \({n_{Cu}} = {n_{CuO}} = a;{\rm{ }}{n_{Cu(N{O_3})}} = b.\)
Khi cho X tan hoàn toàn trong dung dịch H2SO4 thì ta chỉ thu được dung dịch chỉ chứa một chất tan duy nhất nên sau phản ứng thì NO3- hết và muối thu được là CuSO4 .
Ta có : \(CuO + 2{H^ + } \to C{u^{2 + }} + {H_2}O\)
\(\begin{array}{l}
3C{u^{2 + }} + 8{H^ + } + 2N{O^ - } \to 3C{u^{2 + }} + 2NO + 4{H_2}O\\
\,\,a\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\frac{8}{3}a \leftrightarrow 2b
\end{array}\)
\( \to 2a + \frac{8}{3}a = {n_{{H^ + }}} = 2{n_{{H_2}S{O_4}}} = 1,4 \to a = 3\)
Mà \(2b = \frac{2}{3}a \to b = 0,1\)
Vậy khối lượng Cu trong X là : \(\frac{{0,3.64}}{{0,3.(64 + 80) + 0,1.188}} \approx 30,97\% \)

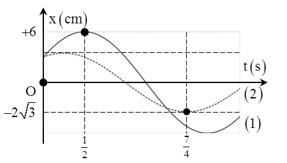
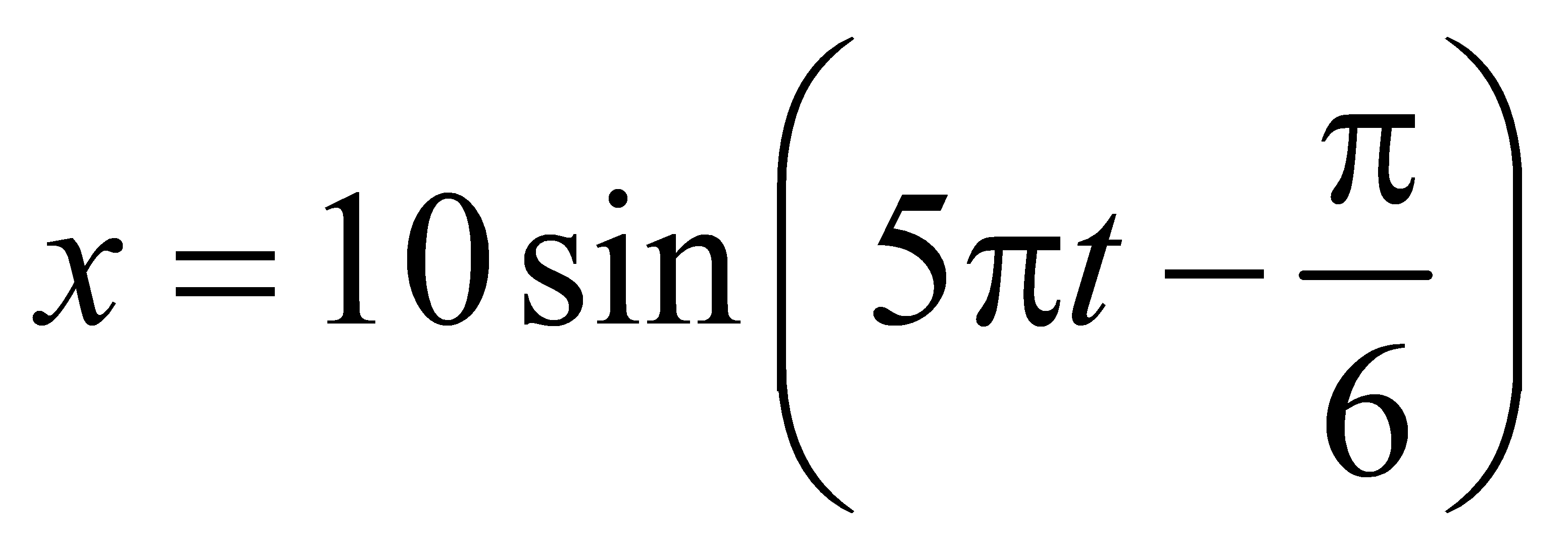 (x đo bằng cm, t đo bằng s). Hãy chọn câu trả lời đúng:
(x đo bằng cm, t đo bằng s). Hãy chọn câu trả lời đúng: