Một hỗn hợp gồm hai đồng vị có số khối trung bình 31,1 và có tỉ lệ phần trăm các đồng vị là 90% và 10%. Tổng số hạt trong hai đồng vị là 93 và tổng số hạt không mang điện bằng 0,55 lần tổng số hạt mang điện. Số nơtron của đồng vị có số khối lớn hơn là
A.16.
B.17.
C.18.
D.19.
Đáp án và lời giải
Đáp án:B
Lời giải:Lời giải: Đặt đồng vị thứ nhất là có số nơtron là N1, đồng vị thứ 2 là có số nơtron là N2 (vì 2 đồng vị thuộc cùng 1 nguyên tố nên Z và E như nhau)
+) Số khối trung bình
. A1 + 0,1. A2 = 31,1
Vì A = Z + N => 0,9. (Z + N1) + 0,1. (Z + N2) = 31,1
=> 100Z + 90N1 + 10N2 = 3110 (1)
+) Tổng số các hạt trong 2 đồng vị là 93:
=> E + Z + N1 + E + Z + N2 = 93
=> (2Z + N1) + (2Z + N2) = 93 => 4Z + N1 + N2 = 93 (2)
+) Tổng số hạt không mang điện bằng 0,55 lần tổng số hạt mang điện
=> N1 + N2 = 0,55. (Z + E + Z + E)
=> N1 + N2 = 0,55. 4Z = 2,2Z (3)
Từ (1), (2) và (3) => Z = 15; N1 = 16; N2 = 17
+) Số khối trung bình
. A1 + 0,1. A2 = 31,1
Vì A = Z + N => 0,9. (Z + N1) + 0,1. (Z + N2) = 31,1
=> 100Z + 90N1 + 10N2 = 3110 (1)
+) Tổng số các hạt trong 2 đồng vị là 93:
=> E + Z + N1 + E + Z + N2 = 93
=> (2Z + N1) + (2Z + N2) = 93 => 4Z + N1 + N2 = 93 (2)
+) Tổng số hạt không mang điện bằng 0,55 lần tổng số hạt mang điện
=> N1 + N2 = 0,55. (Z + E + Z + E)
=> N1 + N2 = 0,55. 4Z = 2,2Z (3)
Từ (1), (2) và (3) => Z = 15; N1 = 16; N2 = 17
Vậy đáp án đúng là B.

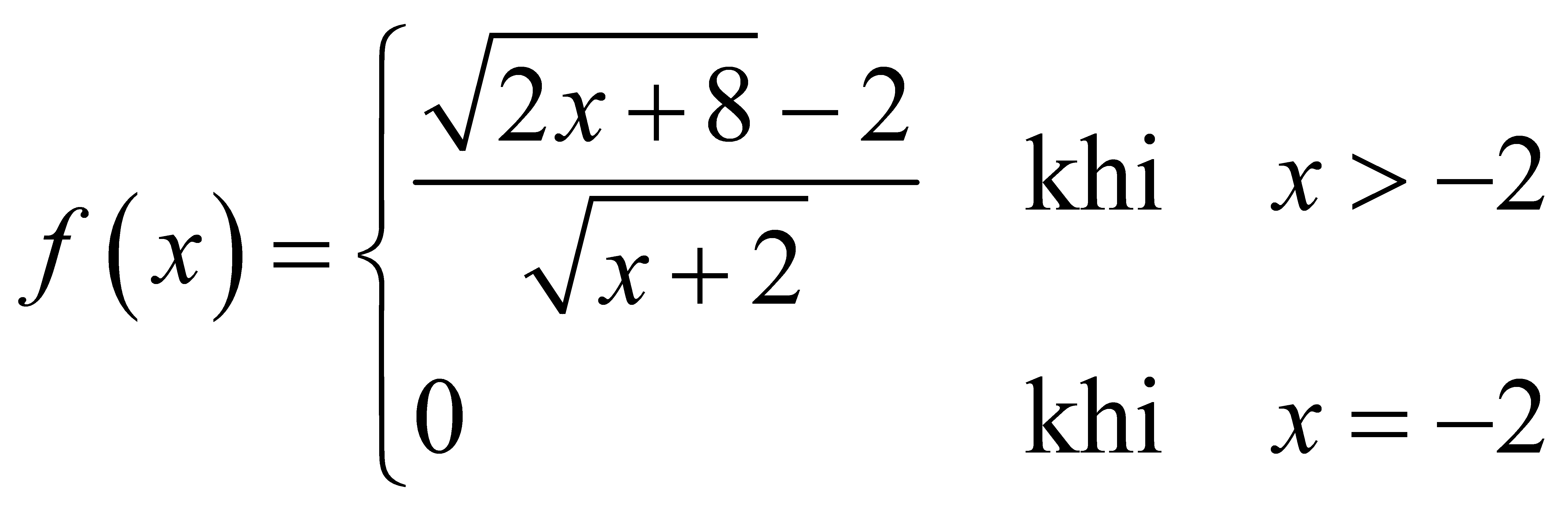 . Tìm khẳng định đúng trong các khẳng định sau
. Tìm khẳng định đúng trong các khẳng định sau 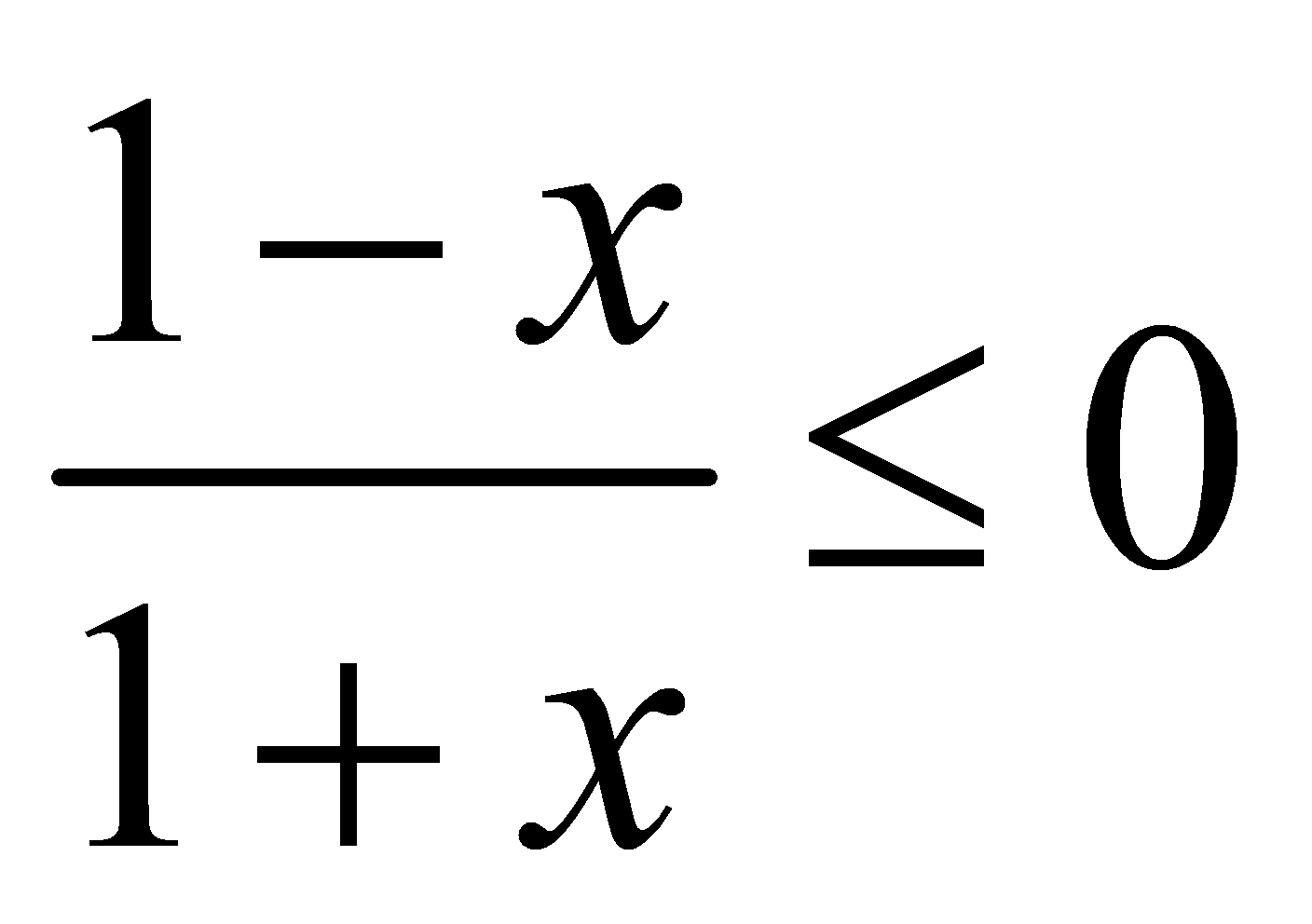 là
là liên tục tại điểm
liên tục tại điểm 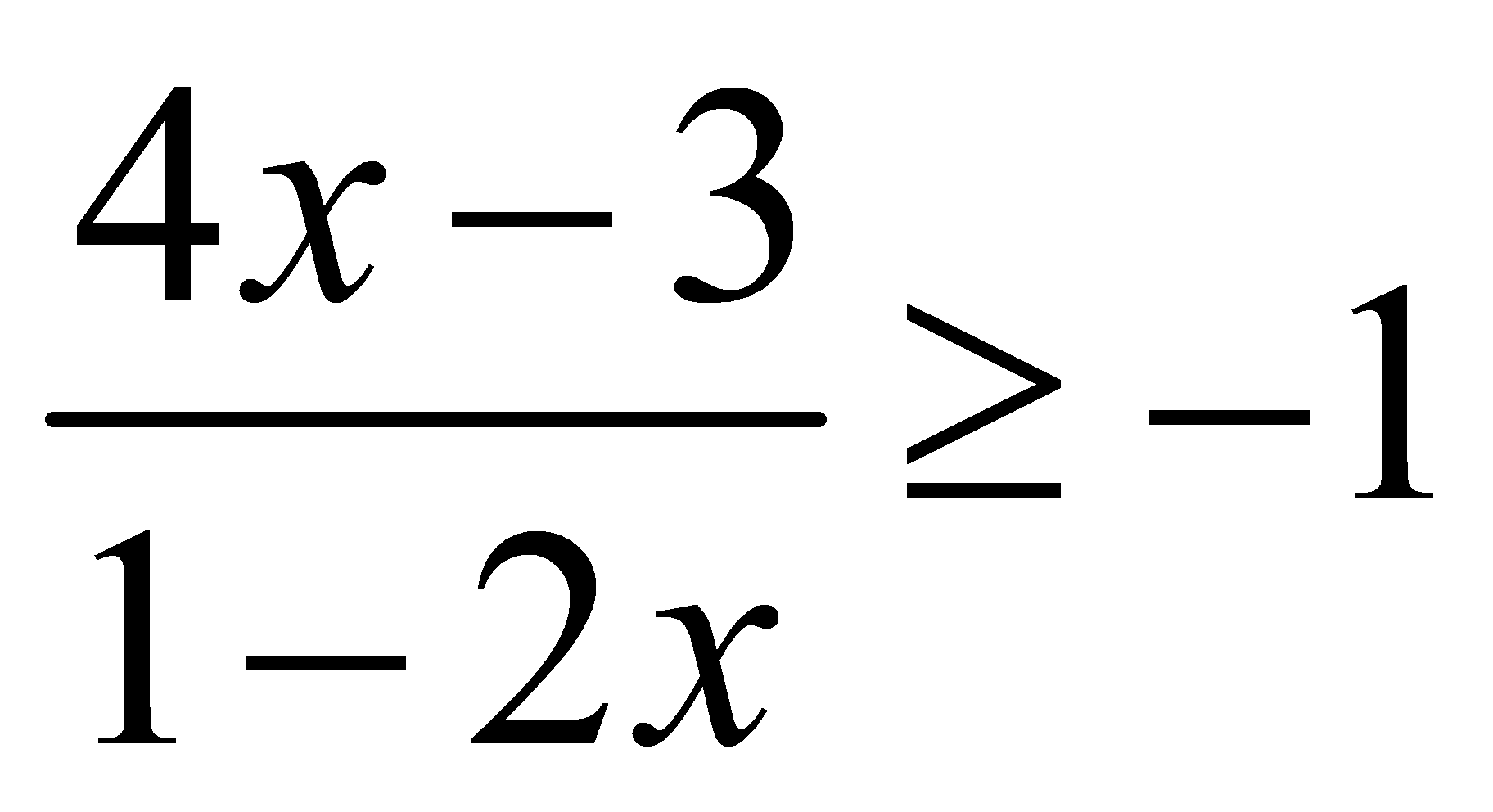 là
là liên tục tại điểm
liên tục tại điểm