X là hỗn hợp gồm hai kim loại Mg và Zn. Y là dung dịch H2SO4 chưa rõ nồng độ.
Thí nghiệm 1: Cho 11,3 gam X vào 1 lít dung dịch Y, sinh ra 3,36 lít H2 (đktc).
Thí nghiệm 2: Cho 11,3 gam X vào 2 lít dung dịch Y sinh ra 6,72 lít H2 (đktc).
Điều khẳng định nào sau đây đúng?
Thí nghiệm 1 X chưa tan hết, thí nghiệm 2 X tan hết.
Thí nghiệm 1 X tan hết, thí nghiệm 2 chưa X tan hết.
Cả thí nghiệm 1 và thí nghiệm 2 X tan hết.
Cả thí nghiệm 1 và thí nghiệm 2 X đều chưa tan hết.
Thí nghiệm 1 X chưa tan hết, thí nghiệm 2 X tan hết.
Đặt nMg = x (mol); nZn = y (mol);
Ta có: 24x + 65y = 11,3 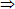
![]() = 0,174 < x + y <
= 0,174 < x + y < ![]() = 0,47 (1)
= 0,47 (1)
Mg + 2H+ ![]() Mg2+ + H2↑ (2)
Mg2+ + H2↑ (2)
Zn + 2H+ ![]() Zn2+ + H2↑ (3)
Zn2+ + H2↑ (3)
Từ (2) và (3) 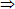
 = nhh phản ứng.
= nhh phản ứng.
TN1: 11,3 (gam) X + 1 lít dung dịch Y (H2SO4):
 =
= ![]() = 0,15 (mol) < 0,174 (mol)
= 0,15 (mol) < 0,174 (mol) 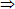 axit hết, kim loại còn dư.
axit hết, kim loại còn dư.
TN2: 11,3 (gam) X + 2 lít dd Y (H2SO4):
 =
= ![]() = 0,3 (mol).
= 0,3 (mol).
Giả sử hỗn hợp 2 kim loại hết, axit vừa hết hoặc còn dư.
Ta có hệ: ![]()
Hệ có nghiệm, nên trong TN2 hỗn hợp kim loại tan hết, axit vừa hết hoặc còn dư.



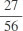
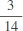
 . Khẳng định đúng trong các khẳng định sau là
. Khẳng định đúng trong các khẳng định sau là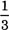 (un + 1). Số hạng u4 có giá trị bằng:
(un + 1). Số hạng u4 có giá trị bằng: