Cho 1,82 gam hỗn hợp bột X gồm Cu và Ag (tỉ lệ số mol tương ứng 4 : 1) vào 30 ml dung dịch gồm H2SO4 0,5M và HNO3 2M, sau khi các phản ứng xảy ra hoàn toàn, thu được a mol khí NO (sản phẩm khử duy nhất của N+5). Trộn a mol NO trên với 0,1 mol O2 thu được hỗn hợp khí Y. Cho toàn bộ Y tác dụng với H2O, thu được 150 ml dung dịch có pH = z. Giá trị của z là:
A.
1
B.
2
C.
3
D.
4
Đáp án và lời giải
Đáp án:A
Lời giải:Gọi a là số mol Ag → nCu = 4a → 108a + 64.4a = 1,82 → a = 0,005 mol. nH2SO4 = 0,015 ; nHNO3 = 0,06 → ∑nH+ = 0,015.2+0,06 = 0,09 ; nNO3- = 0,06 3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O. 0,02...4/75….1/75………………1/75 3Ag + 4H+ + NO3- → 3Ag+ + NO + 2H2O. 0,005…1/150…………………….1/600 →∑nNO = 1/75 + 1/600 = 0,015 2NO + 3/2O2 + H2O → 2HNO3 0,015 0,1 ……………0,015 →[H+] = 0,015/0,15 = 0,1 → pH = -lg0,1 = 1

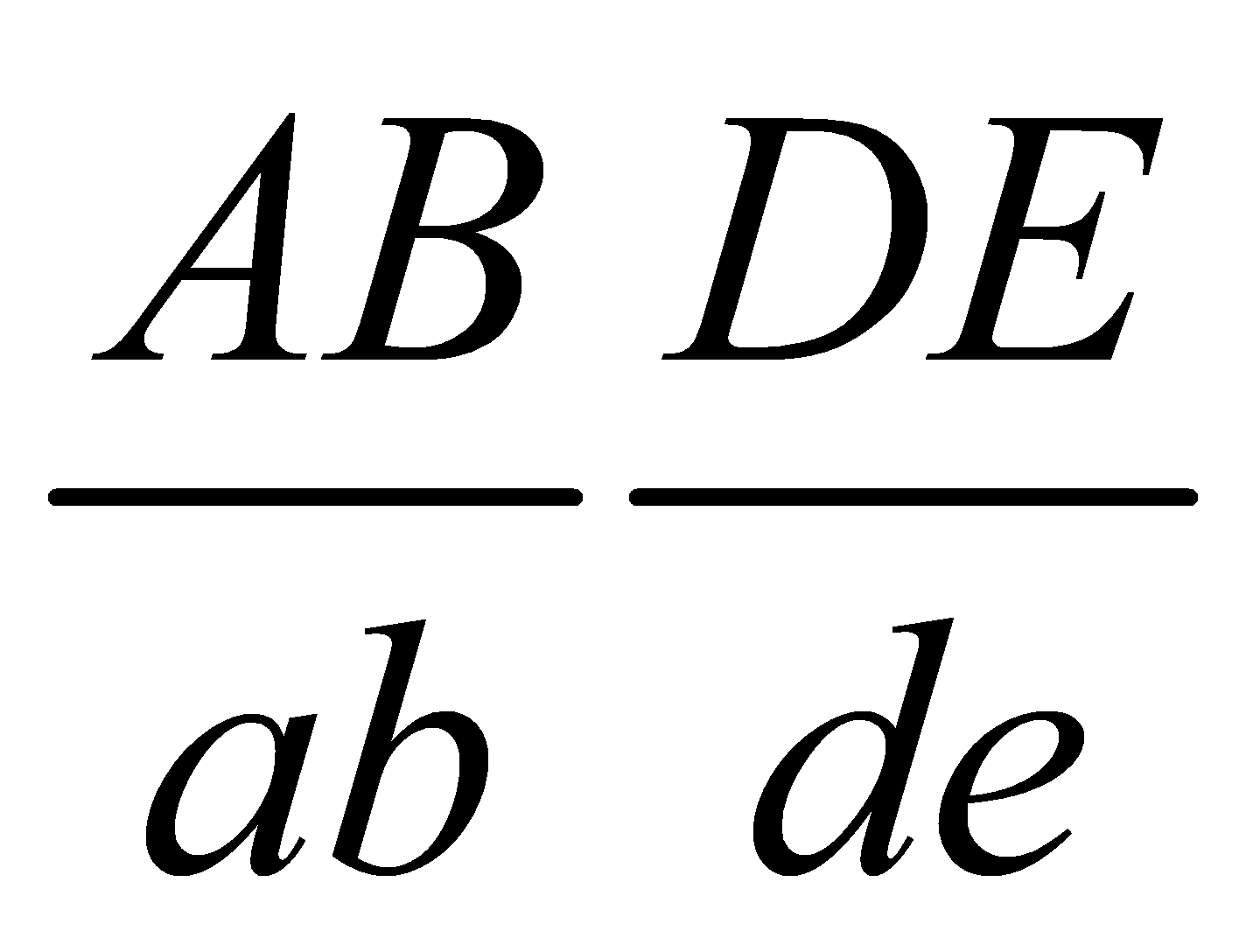 x ♂
x ♂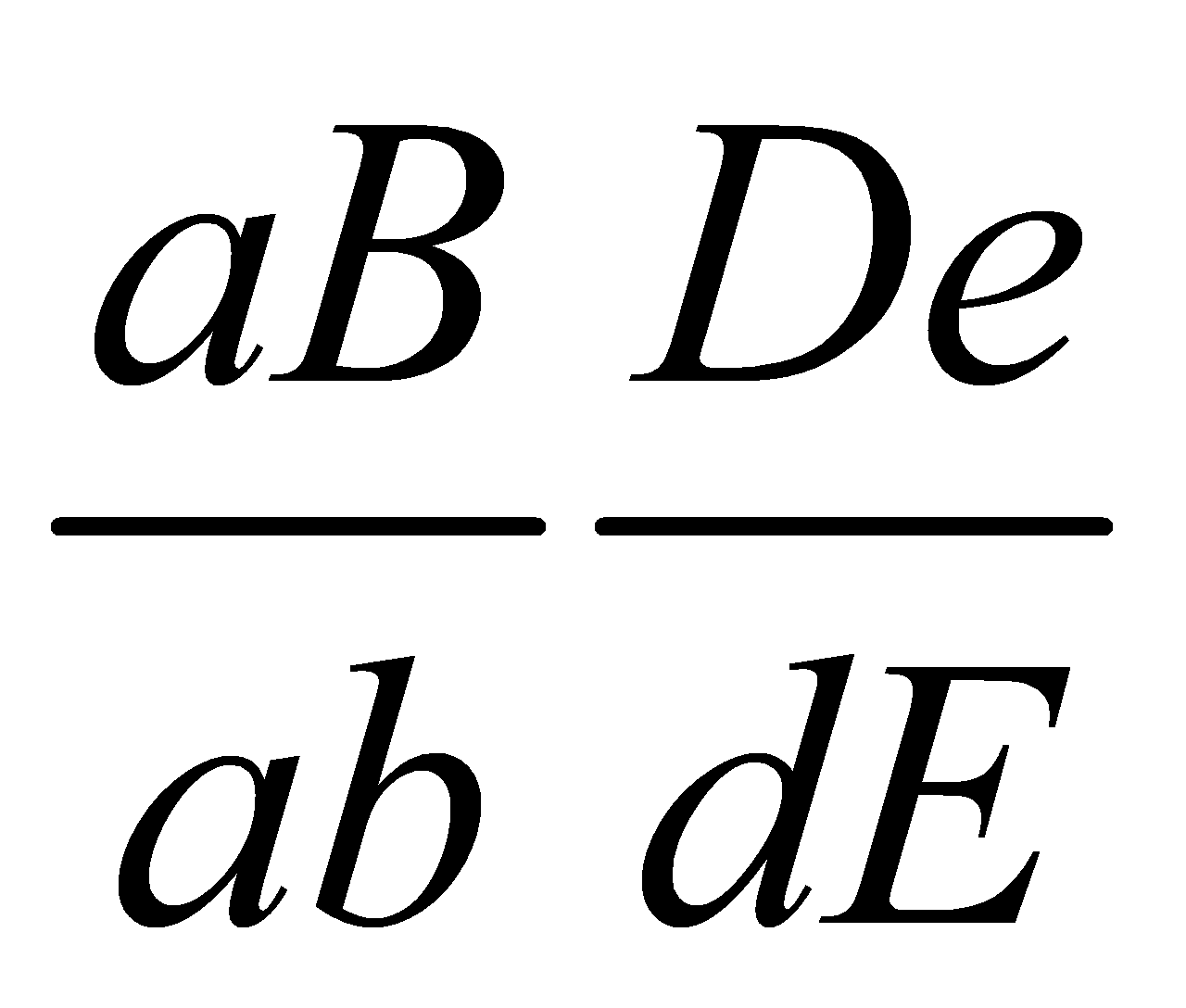 trong trường hợp giảm phân bình thường, quá trình phát sinh giao tử đực và giao tử cái đều xảy ra hoán vị giữa B với b với tần số 20% và D với d đều với tần số 40%. Cho F1 có kiểu hình thân cao, hoa tím, quả tròn, vàng chiếm tỷ lệ:
trong trường hợp giảm phân bình thường, quá trình phát sinh giao tử đực và giao tử cái đều xảy ra hoán vị giữa B với b với tần số 20% và D với d đều với tần số 40%. Cho F1 có kiểu hình thân cao, hoa tím, quả tròn, vàng chiếm tỷ lệ: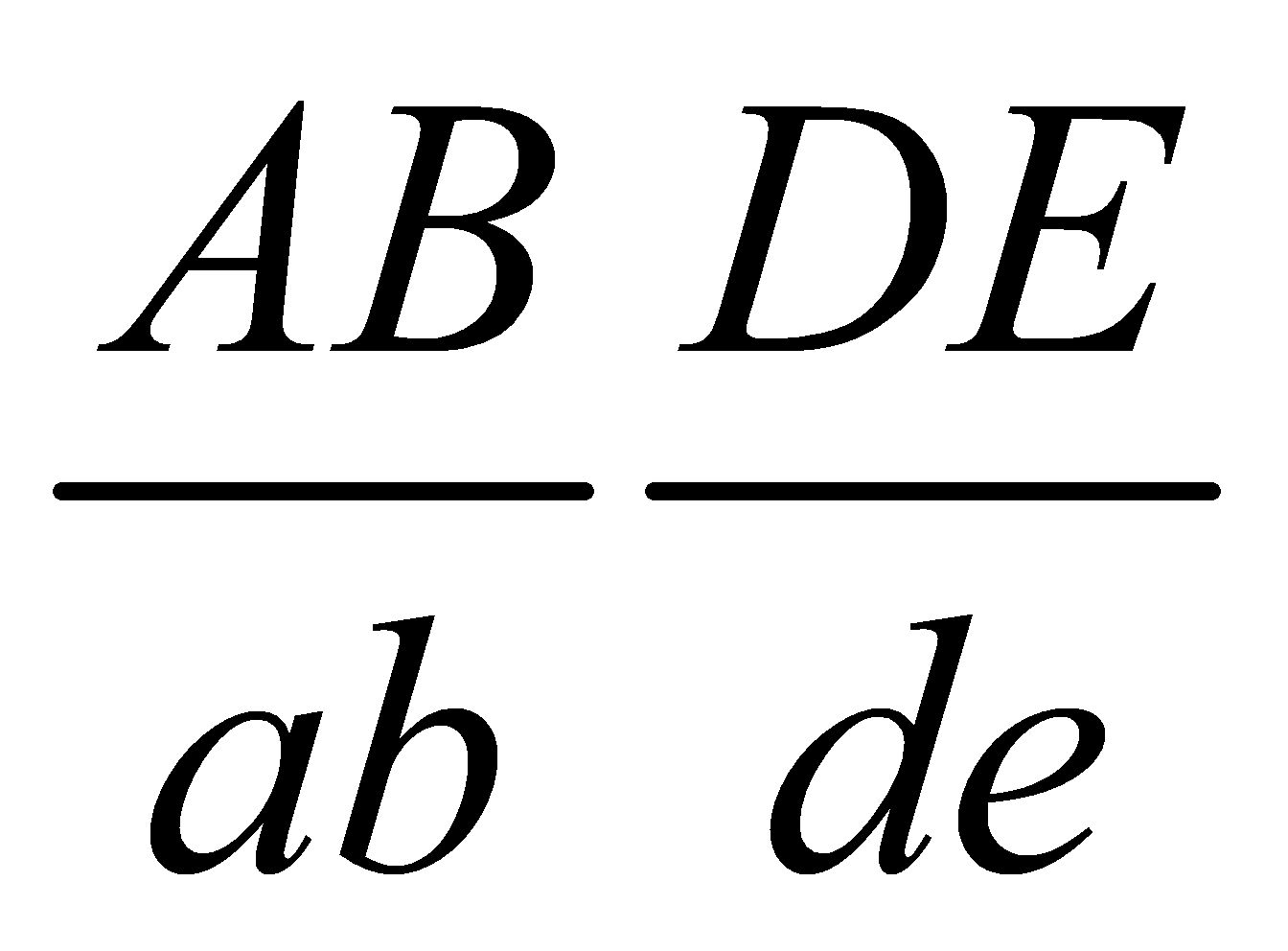 x
x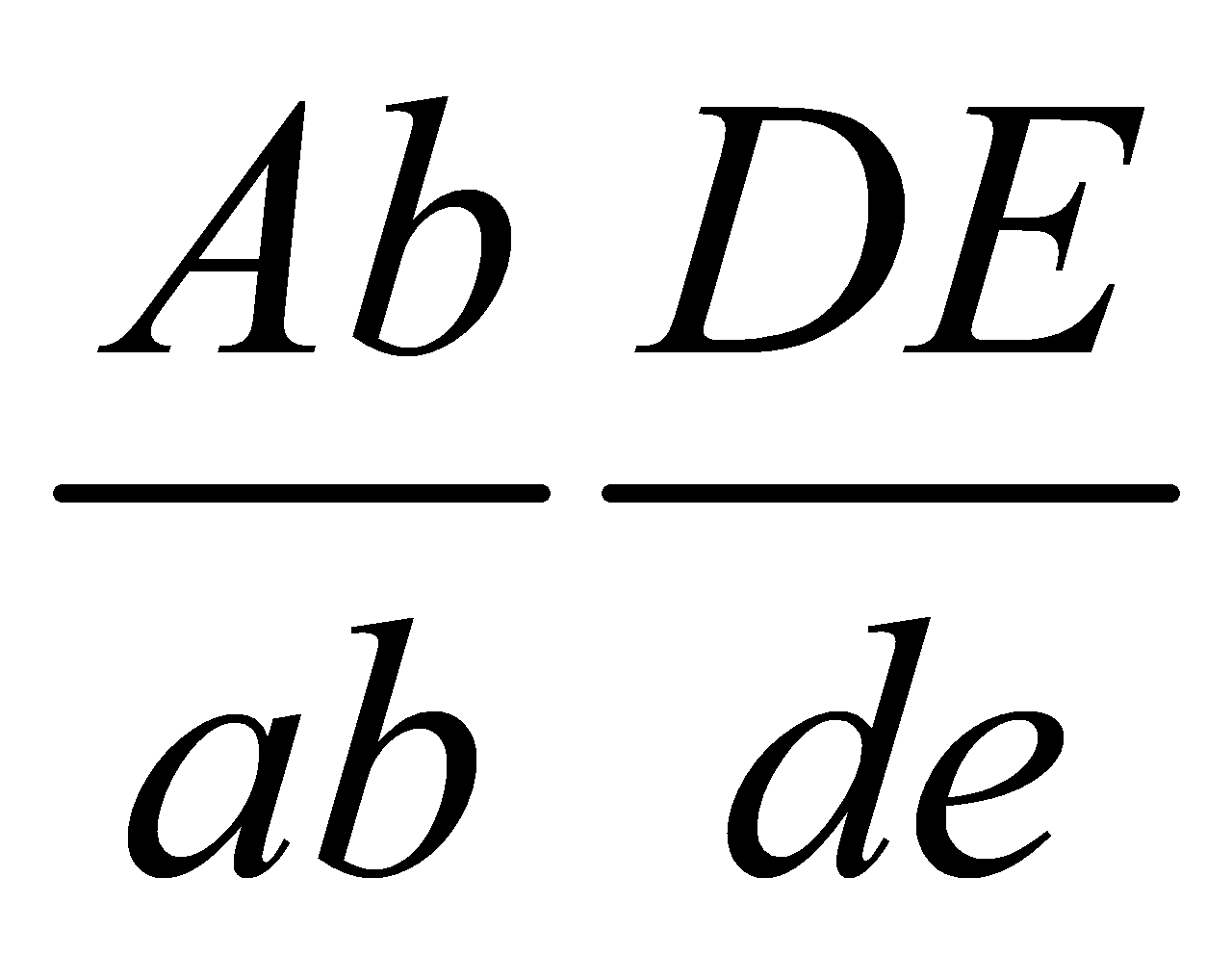 . Nếu xảy ra trao đổi chéo ở cả 2 giới thì số kiểu gen ở F1 là:
. Nếu xảy ra trao đổi chéo ở cả 2 giới thì số kiểu gen ở F1 là: 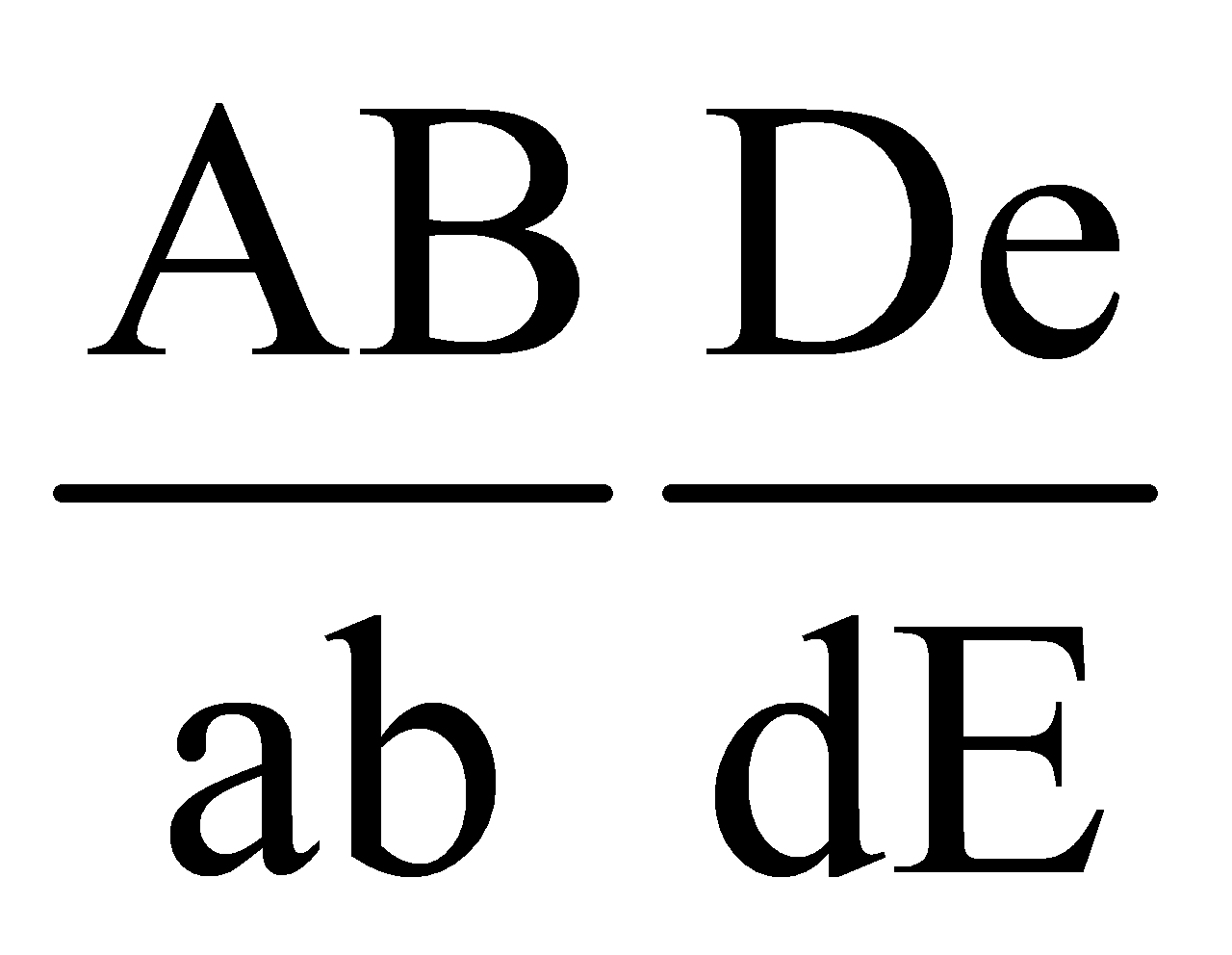 đang tiến hành giảm phân tạo giao tử. Nếu giả sử gen A cách gen B 30cM, gen D cách gen E 20cM thì tính theo lý thuyết. trong số các giao tử được tạo ra, loại giao tử có kiểu gen AB De có tỉ lệ tối đa là:
đang tiến hành giảm phân tạo giao tử. Nếu giả sử gen A cách gen B 30cM, gen D cách gen E 20cM thì tính theo lý thuyết. trong số các giao tử được tạo ra, loại giao tử có kiểu gen AB De có tỉ lệ tối đa là: