Cho m gam Fe vào dung dịch AgNO3 được hỗn hợp X gồm 2 kim loại. Chia X làm 2 phần.
- Phần 1: có khối lượng m1 gam, cho tác dụng với dung dịch HCl dư, được 0,1 mol khí H2.
- Phần 2: có khối lượng m2 gam, cho tác dụng hết với dung dịch HNO3 loãng dư, được 0,4 mol khí NO.
Biết m2 – m1 = 32,8. Giá trị của m bằng:
1,74 gam hoặc 6,33 gam.
33,6 gam hoặc 47,1 gam.
17,4 gam hoặc 63,3 gam.
3,36 gam hoặc 4,71 gam.
Phần 1 : n(Fe) = 0,1 mol , nAg = a mol
Phần 2 : nFe = 0,1n mol và nAg = a.n mol
Ta có :
m2 – m1 = 5,6n + 108a.n – 5,6 – 108.a
= 32,8
=> 5,6.n + 108.a.n – 108 a = 38,4
Mặt khác : Bảo toàn electron ta có 0,3.n + a.n = 1,2 ð
=>n = 3 hoặc n = 108/67
- Khi n = 3 =>a = 0,1
=> Trong X : nFe = 0,4 mol và nAg = 0,4 mol => nFe bđ = 0,4 + 0,2 = 0,6 mol ~ 33,6 gam
- Khi n = 108/67 => a = 4/9
=> Trong X : Fe ( 35/134 mol) , Ag ( 700/603) => Fe(bđ) = 1015/1206 mol ~ 47,131 gam
Vậy đáp án đúng là B

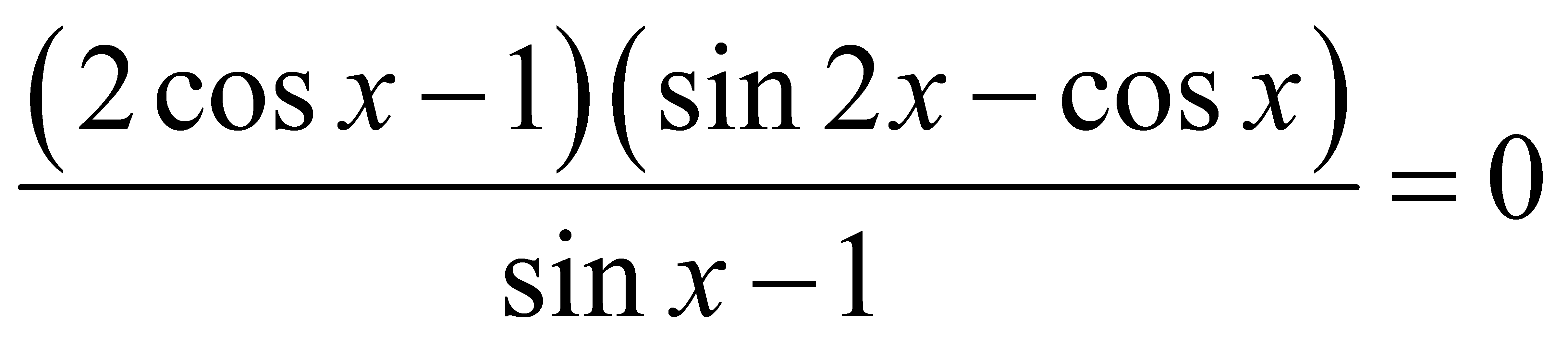 trên
trên 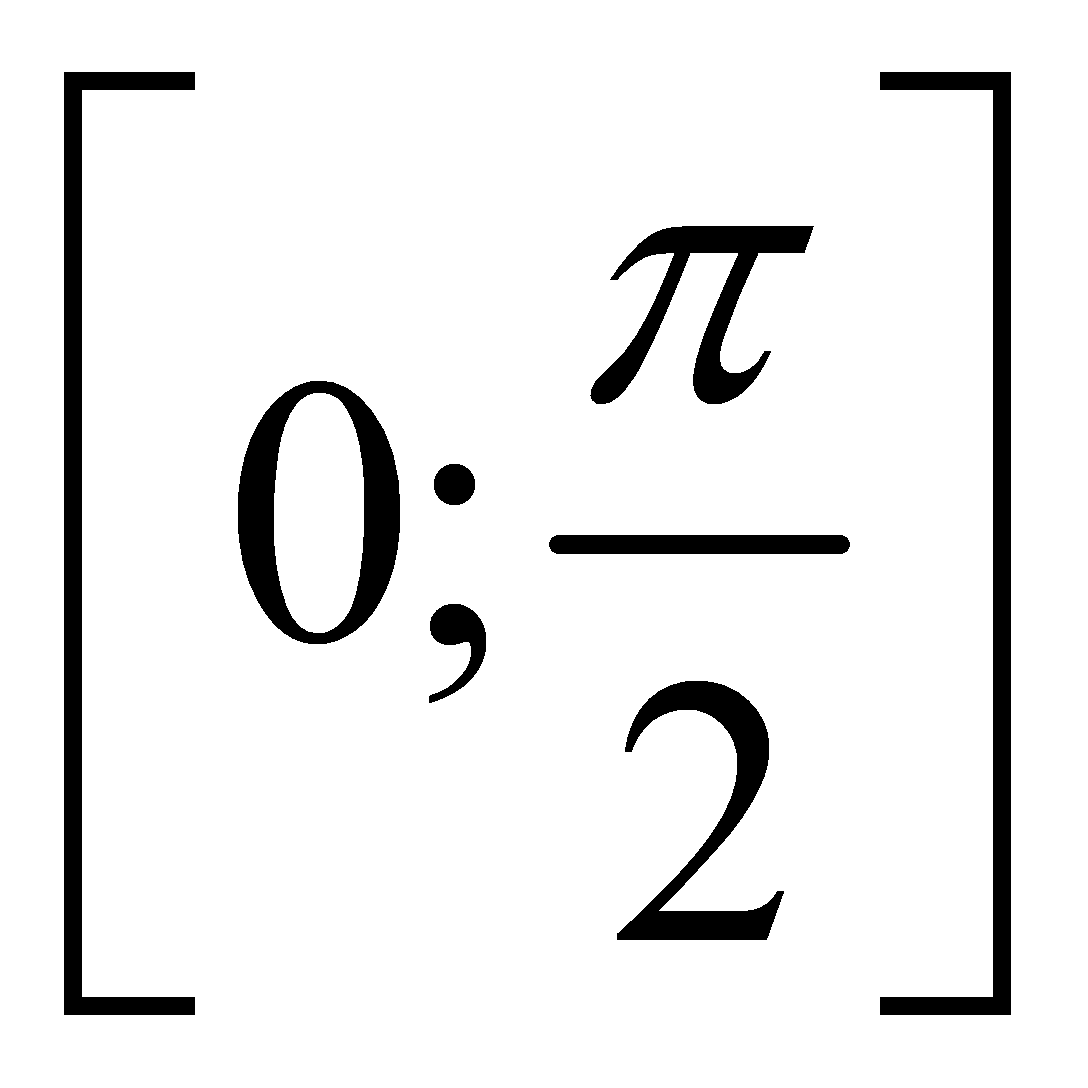 ta được kết quả là:
ta được kết quả là: