Hòa tan hoàn toàn 5,6 gam Fe vào 500ml dung dịch HNO3 thì chỉ thu được dung dịch X và 2,24 lít khí NO duy nhất (đktc). Dung dịch thu được hòa tan tối đa được 5,12 gam Cu. Nồng độ mol của HNO3 ban đầu là:
0,96M.
1,226M.
0,8M.
0,69M.
0,96M.
Fe +4 HNO3 → Fe(NO3)3 + NO +H2O
Ta co nFe= 0,1 mol, nNO=0,1 mol
Vậy Fe phản ứng hết, số mol HNO3 phản ứng là 0,1 x 4 = 0,4 mol.
2Fe(NO3)3 + Cu → 2Fe(NO3)2 + Cu(NO3)2
Ta thấy lượng Cu do Fe(NO3)3 hòa tan được là 0,05 x 64 = 3,2 g.
Vậy 1,92 g Cu được HNO3 dư hòa tan.
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Số mol HNO3 dư là 1,92÷64 x 8÷3 = 0,08 mol
Tổng số mol HNO3 là 0,4 + 0,08 =0,48 mol
Suy ra nồng độ mol./lit của dung dịch HNO3 là 0,48÷0,5 = 0,96 M.

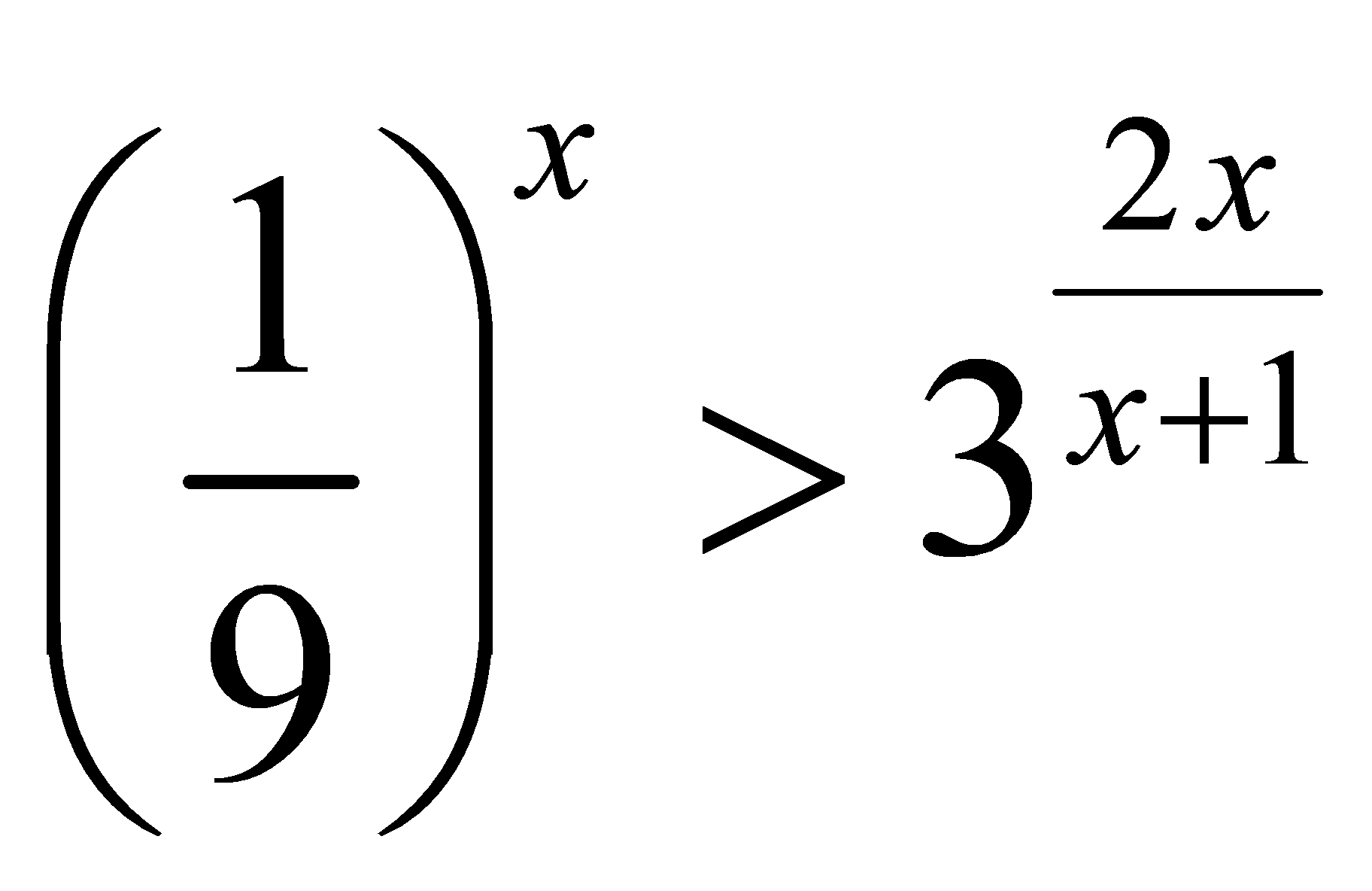 là:
là: