Thực hiện phản ứng nhiệt nhôm (trong điều kiện không có không khí, hiệu suất 100%) với 9,66 gam hỗn hợp X gò Al và một oxit sắt, thu được hỗn hợp rắn Y. Hòa tan Y bằng dung dịch NaOH dư, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Z, chất không tan T và 0,03 mol khí. Sục CO2 đến dư vào dung dịch N, lọc lấy kết tủa nung đến khối lượng không đổi được 5,1 gam một chất rắn. Công thức của oxit sắt và khối lượng của nó trong hỗn hợp X trên là
A. FeO và 7,2 gam.
B. Fe3O4 và 6,96 gam.
C. Fe3O4 và 2,76 gam.
D. Fe2O3 và 8,00 gam.
2yAl + 3FexOy →yAl2O3 + 3xFe(1)
Y + NaOH cho H2 suy ra Y chứa Al dư, Fe và Al2O3 (vì phản ứng xảy ra hoàn toàn)
Y + NaOH: 2Al + 2NaOH + 2 H2O → 2NaAl2O3 + 3H2
Al2O3 + 2 NaOH → 2NaAl2O3 + H2O
Theo phương trình hóa học:
nAl dư 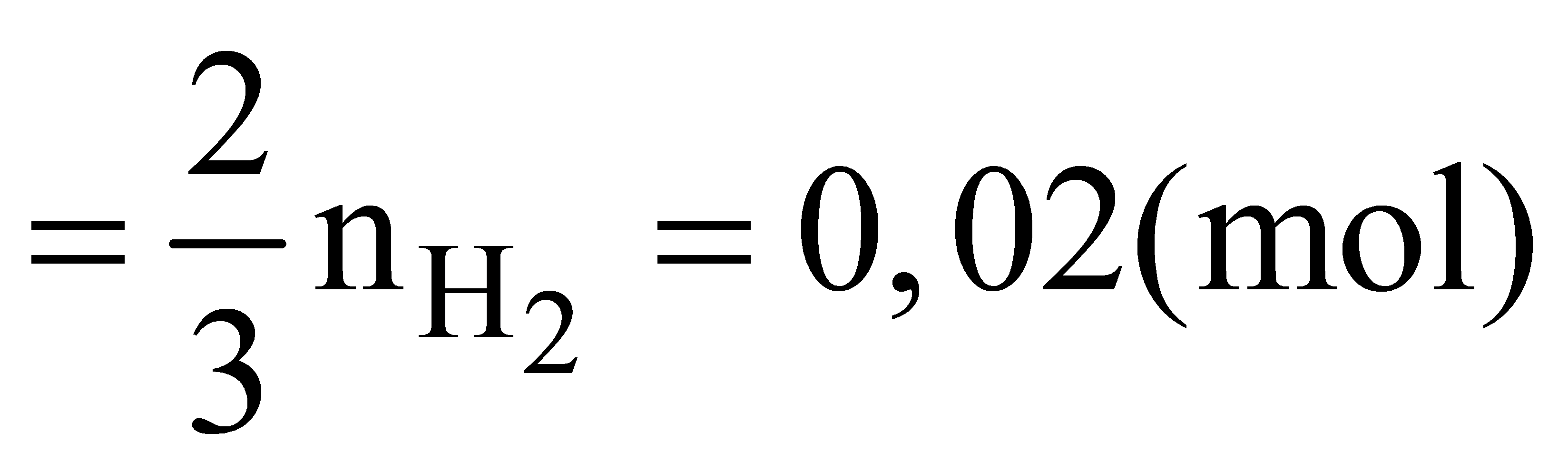
Dung dịch Z gồm NaOH dư và NaAlO2
Dung dịch Z + CO2: NaAlO2 + CO2 + H2O → Al(OH)3 + NaHCO3
2Al(OH)3 → Al2O3 + 3 H2O (2)
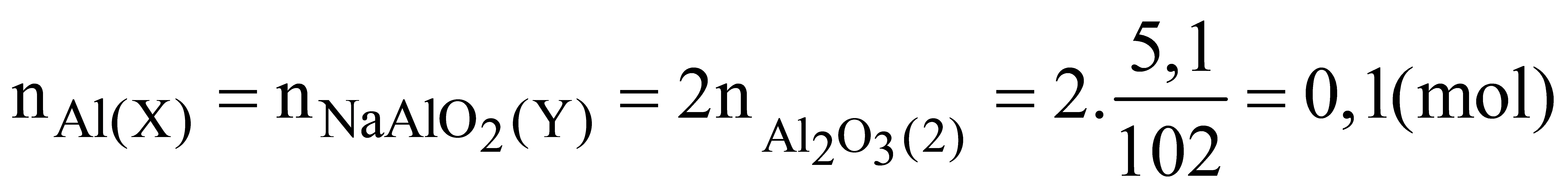
![]()
Dựa vào các phương án trả lời ta được chọn B thỏa mãn
Chú ý: Để tìm oxit sắt ta làm như sau: Số mol Al2O3 sinh ra ở (1): ![]() (nAl (X) – nAl dư) = 0,04 mol
(nAl (X) – nAl dư) = 0,04 mol
Áp dụng định luật bảo toàn khối lượng: ![]() mol
mol
Theo phương trình hóa học (1): 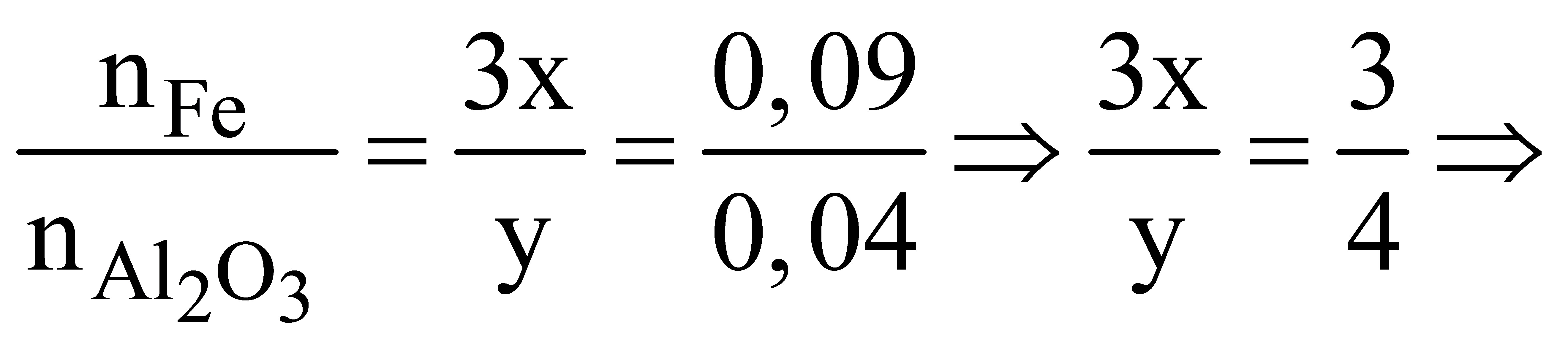 oxit sắt là Fe3O4
oxit sắt là Fe3O4
Vậy đáp án đúng là B

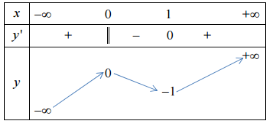 Khẳng định nào sau đây là khẳng định đúng
Khẳng định nào sau đây là khẳng định đúng