Cho 12,6 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 3:2 tác dụng với dung dịch HNO3 loãng, dư thu được dung dịch X và 2,24 lít (đktc) hỗn hợp hai khí không màu,không hóa nâu trong không khí, có tỉ khối hơi so với H2 bằng 18. Số molHNO3 đã tham gia phản ứng là
A: 1,4375 mol
B: 0,9375 mol
C: 1,4750 mol
D: 1,2750 mol
2 khí không màu, không hóa nâu trong không khí là N2 và N2O.
Áp dụng sơ đồ đường chéo ta được: nN2=nN2O=0,05(mol)
mol e nhường > mol e nhận nên phản ứng sinh ra NH4NO3
Áp dụng định luật bảo toàn mol electron ta có: nNH4NO3= (ne Mg + ne Al - ne N2 -neN2O)
Bảo toàn nguyên tố N ta có: nHNO3= nNO3- + 2(nN2+nN2O+nNH4NO3)=1,475(mol)
Vậy đáp án đúng là C

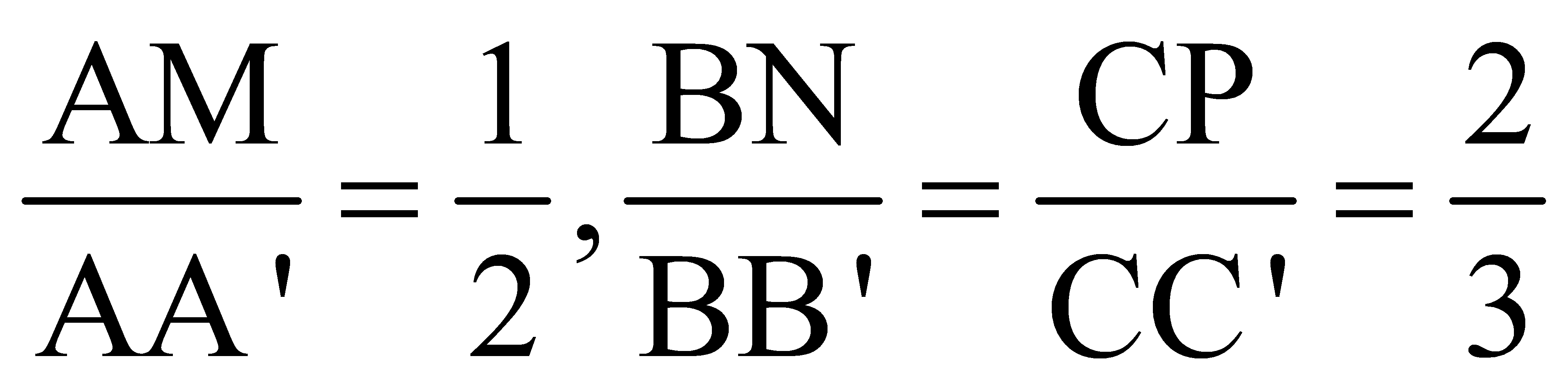 . Thể tích khối đa diện ABC.MNP bằng:
. Thể tích khối đa diện ABC.MNP bằng: 