Tổng số hạt cơ bản trong phân tử X có công thức là M2O là 140, trong phân tử X thì tổng số hạt mang điện nhiều hơn số hạt không mang điện là 44. Vậy X là:
A.K
B.K2O
C.Na2O
D.Cu2O
Đáp án và lời giải
Đáp án:B
Lời giải:Lời giải:
Trong X có 2 nguyên tử M và 1 nguyên tử O.
Nguyên tử O có pO = eO = 8 và nO = 8
Nguyên tử M có pM = eM và nM
=> Tổng số hạt cơ bản trong M2O là: 2. (pM + eM + nM) + pO + eO + nO = 140
=> 2. (2. pM + nM) + 8 + 8 + 8 = 140
=> 4. pM + 2. nM = 116 (1)
Tổng số hạt mang điện trong M2O là: 2. (pM + eM) + 8 + 8 = 4. pM + 16
Tổng số hạt không mang điện trong M2O là: 2. nM + 8
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 44 => 4. pM + 16 – (2. nM + 8) = 44
=> 4. pM – 2. nM = 36 (2)
Từ (1) và (2) ta có: pM = 19; nM = 20
=> M là kim loại K
=> Hợp chất X là: K2O
Đáp án cần chọn là: B
Trong X có 2 nguyên tử M và 1 nguyên tử O.
Nguyên tử O có pO = eO = 8 và nO = 8
Nguyên tử M có pM = eM và nM
=> Tổng số hạt cơ bản trong M2O là: 2. (pM + eM + nM) + pO + eO + nO = 140
=> 2. (2. pM + nM) + 8 + 8 + 8 = 140
=> 4. pM + 2. nM = 116 (1)
Tổng số hạt mang điện trong M2O là: 2. (pM + eM) + 8 + 8 = 4. pM + 16
Tổng số hạt không mang điện trong M2O là: 2. nM + 8
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 44 => 4. pM + 16 – (2. nM + 8) = 44
=> 4. pM – 2. nM = 36 (2)
Từ (1) và (2) ta có: pM = 19; nM = 20
=> M là kim loại K
=> Hợp chất X là: K2O
Đáp án cần chọn là: B
Vậy đáp án đúng là B.

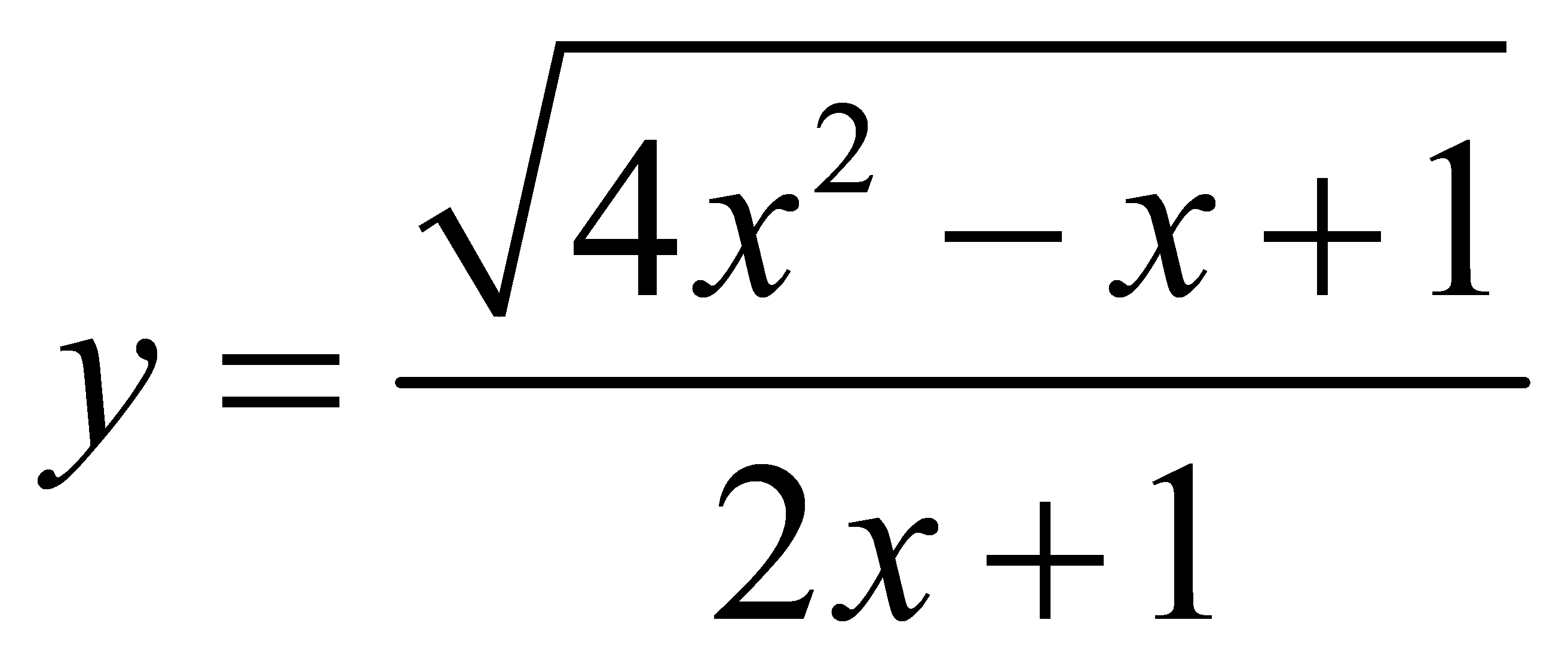 . Tiệm cận ngang của đồ thị hàm số có phương trình là:
. Tiệm cận ngang của đồ thị hàm số có phương trình là: