Nội dung bài giảng
Đun nóng một hỗn hợp bột gồm 2,97 g Al và 4,08 g S trong môi trường kín không có không khí, được sản phẩm rắn là hỗn hợp A. Ngâm A trong dung dịch HCl dư, thu được hỗn hợp khí B.
a) Hãy viết phương trình hóa học của các phản ứng.
b) Xác định thành phần định tính và khối lượng các chất trong hỗn hợp A.
c) Xác định thành phần định tính và thể tích các chất trong hỗn hợp khí B ở điều kiện tiêu chuẩn.
Giải
a) Số mol Al: \({{2,97} \over {27}} = 0,11\,\,mol,\) số mol S: \({{4,08} \over {32}} = 0,1275\,mol\)

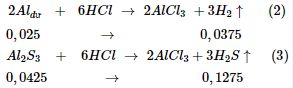
b) Hỗn hợp rắn A: Al2S3 0,0425 mol, Aldư 0,025 mol
Khối lượng các chất trong A:
MAl dư = 0,025.27 = 0,675 (gam), \({m_{A{l_2}{S_3}}} = 0,0425.150 = 6,375\,\,\left( {gam} \right)\)
b) Từ (2) \( \Rightarrow {n_{{H_2}}} = 0,0375\,\,\left( {mol} \right)\)
\(\Rightarrow {V_{{H_2}}} = 0,0375.22,4 = 0,84\,\,\left( {lit} \right)\)
Từ (3) \( \Rightarrow {n_{{H_2}S}} = 0,1275\,\,\left( {mol} \right) \)
\(\Rightarrow {V_{{H_2}S}} = 0,1275.22,4 = 2,856\,\left( {lit} \right)\)

