Nội dung bài giảng
Ở\({550^o}C\), hằng số cân bằng cảu phản ứng sau đây là 0,002:  Người ta cho 0,2 mol C và 1,0 mol \(C{O_2}\) vào một bình kín dung tích 22,4 lít không chứa không khí, nâng dần nhiệt độ trong bình đến \({550^o}C\) và giữa ở nhiệt độ đó đê cân bằng được thiết lập.
Người ta cho 0,2 mol C và 1,0 mol \(C{O_2}\) vào một bình kín dung tích 22,4 lít không chứa không khí, nâng dần nhiệt độ trong bình đến \({550^o}C\) và giữa ở nhiệt độ đó đê cân bằng được thiết lập.
Tính số mol của mỗi chất ở trạng thái cân bằng.
Giải
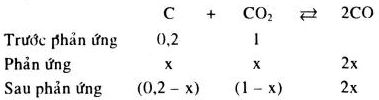
Ta có \({K_c} = \frac{{{{\left[ {CO} \right]}^2}}}{{\left[ {C{O_2}} \right]}} = 0,002.\)
Với \(\left[ {CO} \right] = \frac{{2x}}{V};\left[ {C{O_2}} \right] = \frac{{1 - x}}{V}\)
\( \Rightarrow {\left[ {CO} \right]^2} = {K_C}.\left[ {C{O_2}} \right] \Rightarrow \frac{{4{x^2}}}{{{V^2}}} = {K_c}.\frac{{\left( {1 - x} \right)}}{V}\)
\( \Rightarrow 4{x^2} = {K_c}.V\left( {1 - x} \right)\)
\(\Rightarrow 4{x^2} = 0,002.22,4.\left( {1 - x} \right)\)
\( \Leftrightarrow 625{x^2} + 7x - 7 = 0 \Leftrightarrow x = 0,10\) (nhận) hoặc \(x = - 0,11\) (loại)
Vậy ở trạng thái cân bằng: CO 0,2 mol; \(C{O_2}\) 0,9 mol

