Cho m gam bột Fe vào 800 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và H2SO4 0,25M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,6m gam hỗn hợp bột kim loại và V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của m và V lần lượt là:
17,8 và 4,48.
17,8 và 2,24.
10,8 và 4,48.
10,8 và 2,24.
17,8 và 2,24.
nCu2+= ![]() = 0,2.0,8 = 0,16 (mol)
= 0,2.0,8 = 0,16 (mol)
![]() = 0,25.0,8 = 0,2 (mol)
= 0,25.0,8 = 0,2 (mol) ![]() nH+ = 2.0,2 = 0,4 mol.
nH+ = 2.0,2 = 0,4 mol.
Do sau phản ứng còn hỗn hợp kim loại nên Cu2+ phản ứng hết và Fe bị oxi hóa thành Fe2+
Ta có các quá trình oxi hóa và khử:
![]()
![]()
Từ đó ta có: nNO = ![]() nH+=
nH+= ![]() .0,4 = 0,1 (mol)
.0,4 = 0,1 (mol) ![]() V = 0,1.22,4 = 2,24 (lít)
V = 0,1.22,4 = 2,24 (lít)
Và áp dụng bảo toàn electron ta có:
2nFe = 2nCu2+ + 3nNO ![]() 2a = 2.0,16+ 3.0,1 =0,62
2a = 2.0,16+ 3.0,1 =0,62 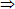 a = 0,31 mol.
a = 0,31 mol.
Ngoài ra từ khối lượng giảm của hỗn hợp kim loại thu được so với lượng Fe ban đầu ta có:
mFe pư - mCu tạo ra = m - 0,6m ![]() 56.0,31 - 64.0,16 = 0,4m
56.0,31 - 64.0,16 = 0,4m 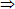 m = 17,8 (g).
m = 17,8 (g).

 . Tích các giá trị cực đại và cực tiểu của hàm số bằng:
. Tích các giá trị cực đại và cực tiểu của hàm số bằng: