Cho m gam hỗn hợp H gồm Al, MgO, AlCl3, Mg(NO3)2 tác dụng vừa đủ với dung dịch chứa 1,38 mo KHSO4, kết thúc phản ứng thu được 0,14 mol NO; 0,04 mol H2; dung dịch X chứa ( m + 173,5) gam muối trung hòa. Cho dung dịch X tác dụng với dung dịch NaOH thì lượng kết tủa thu được là lớn nhất, nung kết tủa đến khối lượng không đổi thu được 29 gam chất rắn. Phần trăm khối lượng AlCl3 trong H có giá trị gần nhất với
A: 33%
B: 22%
C: 34%
D: 25%
Đặt số mol của Al, MgO, AlCl3, Mg(NO3)2 trong H lần lượt là a,b,c,d. Sau phản ứng có khí H2 thoát ra chứng tỏ ![]() phản ứng hết.
phản ứng hết.
![]()
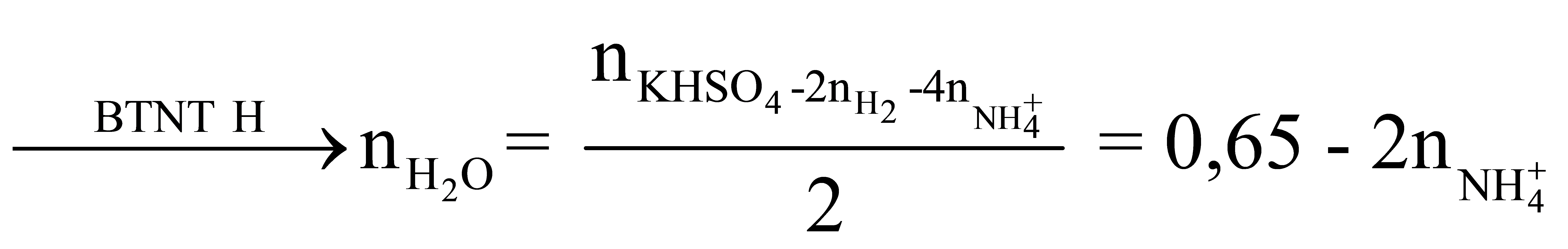
![]()
![]()
![]()
Bảo toàn điện tích trong dung dịch X có: 3a + 2b + 3c + 2.0,095 + 0,05 + 1,38 = 2.1,38 + 3c => b = 0,12
Có m chất rắn = ![]() 102.(0,5a + 0,5c) + 40.(b+0,095) = 29 g. => c = 0,1
102.(0,5a + 0,5c) + 40.(b+0,095) = 29 g. => c = 0,1
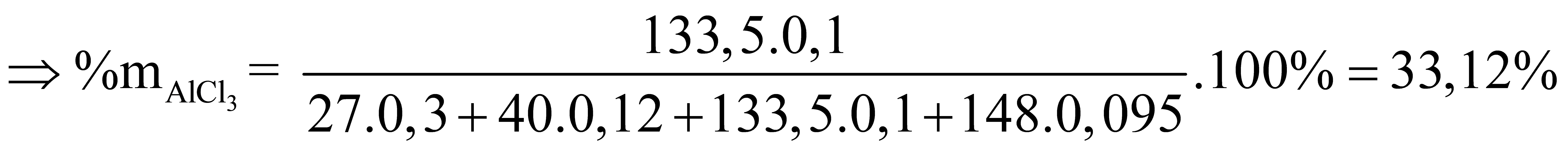
Gần nhất với giá trị 33%
Vậy đáp án đúng là A
