Cho 6,88 gam hỗn hợp chứa Mg và Cu với tỷ lệ mol tương ứng là 1 : 5 vào dung dịch chứa 0,12 mol Fe(NO3)3. Sau khi các phản ứng hoàn toàn thu được m gam kim loại. Giá trị của m là
A: 5,12
B: 3,84
C: 2,56
D: 6,96
- Hướng tư duy 1: Cân bằng phương trình
Mg + 2Fe3+ ![]() Mg2+ + 2Fe2+
Mg2+ + 2Fe2+
mol: 0,02 → 0,04 0,04
Þ ![]() còn lại = 0,08 mol
còn lại = 0,08 mol
Cu + 2Fe3+ ![]() Cu2+ + 2Fe2+
Cu2+ + 2Fe2+
mol: 0,04 ¬ 0,08 Þ nCu dư = 0,06 mol
Vậy mrắn = mCu dư = ![]()
- Hướng tư duy 2: Sử dụng bảo toàn e -
Ta có: ![]() .
.
Nhận thấy: ![]() Þ Fe3+ chỉ về Fe2+.
Þ Fe3+ chỉ về Fe2+.
- Khi đó: nCu dư = 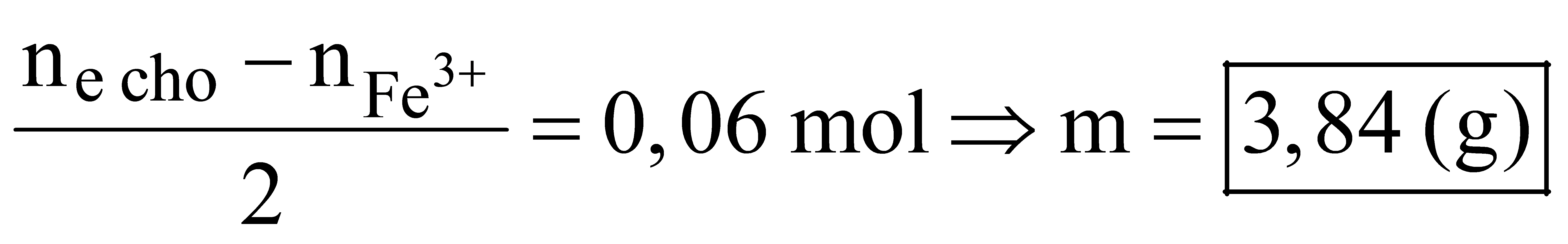
Hướng tư duy 3:

Vậy đáp án đúng là B
