Mắc nối tiếp 2 bình điện phân: bình 1 chứa dung dịch CuCl2, bình 2 chứa dung dịch Na2SO4. Khi ở catôt bình 2 thoát ra 3,2 (g) kim loại thì ở các điện cực khác khối lượng các chất sinh ra là:
Bình 1 gồm catôt 3,20 gam, anôt 3,55 gam; bình 2 gồm catôt 0,1 gam, anôt 0,8 gam.
Bình 1 gồm catôt 3,20 gam, anôt 3,55 gam; bình 2 gồm catôt 0,2 gam, anôt 1,6 gam.
Bình 1 gồm catôt 3,20 gam, anôt 7,10 gam; bình 2 gồm catôt 0,2 gam, anôt 1,6 gam.
Bình 1 gồm catôt 3,20 gam, anôt 7,10 gam; bình 2 gồm catôt 0,05 gam, anôt 0,8 gam.
Bình 1 gồm catôt 3,20 gam, anôt 3,55 gam; bình 2 gồm catôt 0,1 gam, anôt 0,8 gam.
Bình 1: số mol của Cu = ![]() = 0,05 (mol).
= 0,05 (mol).
CuCl2 ![]() Cu + Cl2
Cu + Cl2
Cu2+ + 2e ![]() Cu
Cu
0,1 ← 0,05
2Cl2- + 2e ![]() Cl2
Cl2
0,1 ← 0,05
![]() khối lượng của Cl2: 0,05.71 = 3,55 (g).
khối lượng của Cl2: 0,05.71 = 3,55 (g).
Vì 2 bình điện phân mắc nối tiếp nên số mol electron chuyển qua mỗi bình là bằng nhau = 0,1 mol electron.
Bình 2: Điện phân dung dịch Na2SO4 thực chất là quá trình điện phân của nước.
H2O ![]() H2 + O2
H2 + O2
2H+ + 2e ![]() H2
H2
0,1 → 0,05
2O2- - 4e ![]() O2
O2
0,1 → 0,025
![]() khối lượng của H2: 0,05.2 = 0,1 (g).
khối lượng của H2: 0,05.2 = 0,1 (g).
![]() khối lượng của O2: 0,025.32 = 0,8 (g).
khối lượng của O2: 0,025.32 = 0,8 (g).

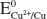 = +0,34 V.
= +0,34 V.